
| A�� | ��������ƽ�����������ϸ���һ�Ŵ�Сһ����ֽ��Ȼ��NaOH�������ֽ�Ͻ��г��� | |
| B�� | �ѳ�����NaOH�������ʢ����������ˮ���ձ��У��ܽ����������Һת�Ƶ�����ƿ�� | |
| C�� | ������ˮϴ���ձ���������2��3�Σ�ÿ��ϴ�Ӻ����Һ��ע������ƿ�� | |
| D�� | ���Ų�����������ƿ�м�������ˮ��ֱ����Һ��Һ��ǡ����̶����� |
���� A��NaOH�׳��⣬���и�ʴ�ԣ�
B��Ӧ��ȴ��ת�ƣ�
C���ձ���������ϴ�ӣ�����������ʣ�
D������ʱ��ˮ���̶���1��2cm�������ý�ͷ�ιܵμӣ�
��� �⣺A��NaOH�׳��⣬���и�ʴ�ԣ���Ӧ��NaOH��С�ձ��г�������A����
B��Ӧ��ȴ��ת�ƣ������ܽ����������Һת�Ƶ�����ƿ�У���B����
C���ձ���������ϴ�ӣ�����������ʣ���������ˮϴ���ձ���������2��3�Σ�ÿ��ϴ�Ӻ����Һ��ע������ƿ�У���C��ȷ��
D������ʱ��ˮ���̶���1��2cm�������ý�ͷ�ιܵμӣ�����Һ��Һ��ǡ����̶����У���D����
��ѡC��
���� ���⿼����Һ�����ƣ�Ϊ��Ƶ���㣬����������Һ�IJ�����������ʵ�鼼��Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע��ʵ�������������Ŀ�ѶȲ���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
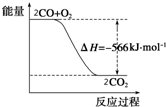 ��֪��2CO��g��+O2��g���T2CO2��g����H=-566kJ•mol-1
��֪��2CO��g��+O2��g���T2CO2��g����H=-566kJ•mol-1| A�� | CO��ȼ����Ϊ566 kJ•mol-1 | |
| B�� | ��ͼ�ɱ�ʾ��CO����CO2�ķ�Ӧ�����������仯�Ĺ��� | |
| C�� | 2Na2O2��s��+2CO2��s���T2Na2CO3��s��+O2��g����H=-452 kJ/mol | |
| D�� | CO��g����Na2O2��s����Ӧ�ų�509 kJ����ʱ������ת����Ϊ2 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| t�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����� | B�� | ������ | C�� | ��ԭ�� | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
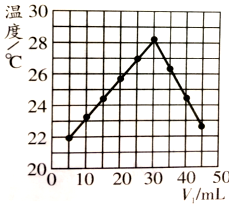
| A�� | ʵ�����ʱ�Ļ����¶�Ϊ22�� | |
| B�� | ʵ��������ܿ�ת��Ϊ��ѧ�� | |
| C�� | ��ʵ�������ˮ���ɵķ�Ӧ���Ƿ��ȷ�Ӧ | |
| D�� | NaOH��Һ��Ũ��ԼΪ1.50 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
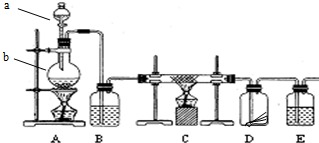
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
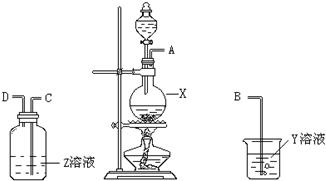 ij��ѧ������ȤС��Ϊ̽��ͭ��Ũ���ᷴӦ��������ʣ�������ͼ��ʾ��װ�ý���ʵ�飮
ij��ѧ������ȤС��Ϊ̽��ͭ��Ũ���ᷴӦ��������ʣ�������ͼ��ʾ��װ�ý���ʵ�飮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | �ۢ� | D�� | �٢ڢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com