
| A、28gCO和N2的混合气体中含有原子总数为2NA |
| B、常温常压下,2g氢气所含原子数目为2NA |
| C、标准状况下,足量Fe与22.4LCl2反应,转移电子数为2NA |
| D、0.1mol/LNa2CO3溶液中含有的Na+数目为0.2NA |


 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案科目:高中化学 来源: 题型:
| A、非金属原子间以共价键结合的物质都是共价化合物 |
| B、含有共价键的化合物都是共价化合物 |
| C、凡是能电离出离子的化合物都是离子化合物 |
| D、氮、氧、氟的氢化物分子间可以形成氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、①②③④ | B、③⑦ |
| C、①③④⑤ | D、①④⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
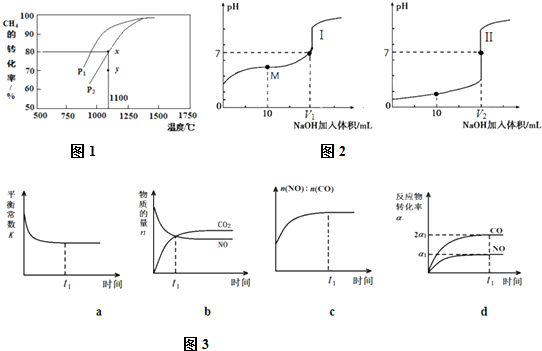
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1mol CO2(g)和3mol H2(g) | 1mol CH3OH(g)和1mol H2O(g) |
| 平衡时c(CH3OH) | c1 | c2 |
| 平衡时能量变化 | 放出29.4kJ | 吸收a kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 R1-CHO+R2-CHO
R1-CHO+R2-CHO
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水电离的c(H+):①=②=③=④ |
| B、若将②、③溶液混合后,pH=7,则消耗溶液的体积:②=③ |
| C、等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:①最大 |
| D、向溶液中加入100mL水后,溶液的pH:③>④>②>① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com