
іЈОВПВKMnO4Сх»ҜЕЁHClөД·ҙУҰ·ҪіМКҪИзПВЈә2KMnO4 Ј«16HClЈЁЕЁЈ©=2KClЈ«2MnCl 2Ј«5Cl 2ЎьЈ«8H2O
ЈЁ1Ј©УГЎ°Л«ПЯЗЕ·ЁЎұұкГч·ҙУҰЦРөзЧУЧӘТЖөД·ҪПтәНКэДҝЎЈ
ЈЁ2Ј©УЦТСЦӘ Ј¬ҪбәПТФЙП·ҙУҰФӯАнЈ¬ФтMnO2ЎўKMnO4ЎўCl2өДСх»ҜРФУЙЗҝөҪИхөДЛіРтКЗЈә ЎЈ
Ј¬ҪбәПТФЙП·ҙУҰФӯАнЈ¬ФтMnO2ЎўKMnO4ЎўCl2өДСх»ҜРФУЙЗҝөҪИхөДЛіРтКЗЈә ЎЈ
ЈЁ3Ј©ИфУР63.2gёЯГМЛбјШІОјУ·ҙУҰЈ¬Фтұ»Сх»ҜөДHClөДОпЦКөДБҝОӘ molЈ¬ІъЙъөДCl2ФЪұкЧјЧҙҝцПВөДМе»эОӘ LЎЈ
ЈЁ1Ј©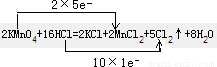 ЈЁ2Ј©KMnO4 MnO2 Cl2 ЈЁ3Ј©2 22.4
ЈЁ2Ј©KMnO4 MnO2 Cl2 ЈЁ3Ј©2 22.4
ЎҫҪвОцЎҝ
КФМв·ЦОцЈәЈЁ1Ј©Л«ПЯЗЕ·Ёұкіц·ҙУҰЦРөзЧУөГК§КэДҝОӘ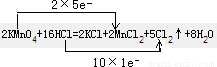 Ј»
Ј»
ЈЁ2Ј©2KMnO4 Ј«16HClЈЁЕЁЈ©=2KCl Ј«2MnCl 2Ј«5Cl 2Ўь Ј«8H2OҙЛ·ҙУҰЦЖИЎCl2І»РиТӘМхјюЈ¬¶шФЪ·ҙУҰ ЦРТӘјУИИЈ¬ЗТMnO2 КЗСх»ҜјБЈ¬ Cl2КЗСх»ҜІъОпЎЈЛщТФУРСх»ҜРФKMnO4 >MnO2 >Cl2
ЦРТӘјУИИЈ¬ЗТMnO2 КЗСх»ҜјБЈ¬ Cl2КЗСх»ҜІъОпЎЈЛщТФУРСх»ҜРФKMnO4 >MnO2 >Cl2
ЈЁ3Ј©ёЯГМЛбјШөДБҝЎўВИЖшөДБҝТФј°ПыәДөДСОЛбЦ®јдөД№ШПөОӘЈә2KMnO4Ў«5Cl2Ў«16HClЈ¬ұ»Сх»ҜөДСОЛбәНІОјУ·ҙУҰөДСОЛбөДБҝЦ®ұИОӘЈә10 :16 ЈҪ5 :8 Ј¬63.2g ЈЁјҙ0.4molЈ©KMnO4НкИ«·ҙУҰКұЈ¬ІъЙъөДCl2ОӘ1.0molЈ¬ФЪұкЧјЧҙҝцПВөДМе»эОӘ1.0molЎБ22.4L/mol=22.4LЈ¬ПыәДөДHClОӘ3.2molЈ¬ұ»Сх»ҜөДHClОӘ2.0mol.
ҝјөгЈәұҫМвҝјІйСх»Ҝ»№Фӯ·ҙУҰЦРөДУР№ШёЕДоәНөзЧУЧӘТЖЦӘК¶



| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2016ҪмёКЛаКЎјОУш№ШКРёЯТ»ЙПС§ЖЪЖЪЦРҝјКФ»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
ПВБРёчИЬТәЦРЈ¬c( Na+ ) ЧоҙуөДКЗЈЁ Ј©
AЎў4L 0.5mol/LөДNaClИЬТә BЎў2L 0.8mol/LөДNaOHИЬТә
CЎў1L 1mol/LөДNa2CO3ИЬТә DЎў0.5L 1.2mol/LөДNa2SO4ИЬТә
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2016ҪмёКЛаКЎёЯТ»ЙПС§ЖЪЖЪД©ҝјКФ»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
ПВБР»ҜәПОпІ»ДЬУЙБҪЦЦөҘЦКЦұҪУ»ҜәП¶шіЙөДКЗ( )ЎЈ
AЈ®FeCl2 BЈ®Na2SCЈ®FeCl3 DЈ®SO2
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2016ҪмәюұұКЎёЯТ»ЙПС§ЖЪЖЪД©ҝјКФ»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
ФЪ200mLВИ»ҜГҫәНВИ»ҜВБөД»мәПТәЦРЈ¬Mg2+өДОпЦКөДБҝЕЁ¶ИОӘ0.2mol/LЈ¬Cl-өДОпЦКөДБҝЕЁ¶ИОӘ1.3 mol/LЎЈТӘК№Mg2+И«ІҝЧӘ»ҜОӘіБөн·ЦАліцАҙЈ¬ЦБЙЩРиТӘјУИл4 mol/L NaOHИЬТәөДМе»эОӘ
AЈ®80mL BЈ®128mL CЈ®40mL DЈ®72mL
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2016ҪмәюұұКЎёЯТ»ЙПС§ЖЪЖЪД©ҝјКФ»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
ПВБРРрКцХэИ·өДКЗ
ўЩNa2OУлNa2O2¶јДЬәНЛ®·ҙУҰЙъіЙјоЈ¬ЛьГЗ¶јКЗјоРФСх»ҜОп
ўЪNa2OУлCO2·ўЙъ»ҜәПЙъіЙNa2CO3Ј¬Na2O2УлCO2·ўЙъЦГ»»ЙъіЙO2
ўЫNa2OКЗөӯ»ЖЙ«ОпЦКЈ¬Na2O2КЗ°ЧЙ«ОпЦК
ўЬNa2O2ҝЙЧч№©СхјБЈ¬¶шNa2OІ»РР
ўЭNa2O2әНNa2OСжЙ«·ҙУҰҫщОӘ»ЖЙ«
AЎў¶јХэИ· BЎўўЪўЫўЬўЭ CЎўўЪўЫўЭ DЎўўЬўЭ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2016ҪмәюұұКЎёЯТ»ЙПС§ЖЪЖЪЦРҝјКФ»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәМоҝХМв
ўЕПВБРОпЦКЈәўЩИЫИЪВИ»ҜДЖ ўЪСОЛб ўЫҙҝҙЧЛб(CH3COOH) ўЬМјЛбёЖ ўЭҫЖҫ« ўЮ¶юСх»ҜМј ўЯБтЛбЗвДЖ№ММе ўаНӯ ўбМјЛбЗвДЖ№ММе ўвЗвСх»ҜұөИЬТәЈ¬КфУЪөзҪвЦКөДКЗ Ј¬ КфУЪ·ЗөзҪвЦКөДКЗ Ј¬ДЬөјөзөДКЗ ЎЈЈЁУГРтәЕМоҝХЈ©
ўЖРҙіцОпЦКўЫәНўбФЪЛ®ЦР·ҙУҰөДАлЧУ·ҪіМКҪЈә ЎЈ
ўЗҪ«ОпЦКўЯЕдЦЖіЙИЬТәЈ¬ЦрөОөОИлўвЦРЦБBa2+ЗЎәГіБөнНкИ«Ј¬РҙіцАлЧУ·ҪіМКҪЈә ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2016ҪмәюұұКЎёЯТ»ЙПС§ЖЪЖЪЦРҝјКФ»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
КөСйКТУГ№ММ¬І»ҙҝВИ»ҜДЖЈЁә¬ЙЩБҝNH4HCO3әНNa2SO4ФУЦКЈ©ЕдЦЖВИ»ҜДЖИЬТәЎЈПВБРІЩЧчҝЙ№©СЎУГЈәўЩЦрөОјУИлПЎСОЛбЈ¬өчҪЪpHЦөОӘ5Ј»ўЪЦу·РЈ»ўЫјУХфБуЛ®ИЬҪвЈ»ўЬјУИИЦБІ»ФЩІъЙъЖшМеОӘЦ№Ј»ўЭјУИлЙФ№эБҝөДNa2CO3ИЬТәЈ»ўЮјУИлЙФ№эБҝөДBaCl2ИЬТәЈ»ўЯ№эВЛЎЈЙПКцКөСйІЩЧчөДХэИ·ЛіРтУҰКЗЈЁ Ј©
AЈ®ўЩўЪўЭўЮўЯўЫўЬ BЈ®ўЫўЬўЮўЭўЯўЩўЪ
CЈ®ўЬўЫўЮўЭўЯўЩўЪ DЈ®ўЬўЫўЭўЮўЯўЪўЩ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2016ҪмәюұұКЎёЯТ»ЙПС§ЖЪЖЪЦРҝјКФ»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
ПВБРАлЧУ·ҪіМКҪУлЛщКцКВКөПа·ыЗТХэИ·өДКЗЈЁ )
AЈ®Ca(OH)2РьЧЗТәЦРөОјУЧгБҝПЎПхЛбЈәHЈ«Ј«OHЈӯ=H2O
BЈ®Ca(HCO3)2ИЬТәЦРјУИлЙЩБҝNaOHИЬТәЈәCa2Ј«Ј«2HCO3ЈӯЈ«2OHЈӯЈҪCaCO3ЎэЈ«CO32ЈӯЈ«H2O
CЈ®БтЛбЗвДЖИЬТәЦРјУИлBa(OH)2ИЬТәЦБSO42ЈӯЗЎәГНкИ«іБөнЈә2HЈ«Ј«SO42ЈӯЈ«Ba2Ј«Ј«2OHЈӯЈҪBaSO4ЎэЈ«2H2O
DЈ®Птә¬УР0.4 mol FeBr2өДИЬТәЦРНЁИл0.3 mol Cl2ід·Ц·ҙУҰЈә4Fe2Ј«Ј«2BrЈӯЈ«3Cl2ЈҪ4Fe3Ј«Ј«6ClЈӯЈ«Br2
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2016ҪмәЈДПКЎЗнәЈКРёЯТ»ЙПС§ЖЪ¶Оҝј»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәМоҝХМв
ЈЁ1Ј©0Ј®5molCH4өДЦКБҝКЗ gЈ¬ФЪұкЧјЧҙҝцПВөДМе»эОӘ LЈ»ә¬ УРФј ёцЗвФӯЧУЎЈ
Ҫ«ұкЧјЧҙҝцПВ22Ј®4 LөДHClИЬУЪЛ®ЕдіЙ200 mLөДИЬТәЈ¬ЛщөГИЬТәөДОпЦКөДБҝЕЁ¶ИОӘ Ј»ЕдЦЖ300 mL 0Ј®5 molЎӨLЈӯ1ВИ»ҜДЖИЬТәЈ¬РиТӘ1Ј®5 molЎӨLЈӯ1өДВИ»ҜДЖИЬТәөДМе»эКЗ mLЎЈ
Ійҝҙҙр°ёәНҪвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com