
【题目】下列实验试剂保存正确的是( )
A.将氢氟酸保存在玻璃细口瓶中B.将金属钠保存在冷水中
C.保存 NaOH 的试剂瓶使用橡胶塞D.将金属锂保存在煤油中
科目:高中化学 来源: 题型:
【题目】有五种物质是①6gH2;②0.5molCO2;③1.204×1024个HCl;④147g硫酸;⑤92g乙醇(C2H5OH),它们的物质的量最大的是____,所含分子数最多的是____,含有原子个数最多的是___,质量最大的是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化钙(Ca3N2)是一种重要的化工试剂,遇水剧烈水解。实验室可由氮气和钙加热制得氮化钙,实验装置如下图(省略部分固定装置)。
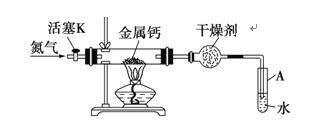
(1)氮化钙中所含的化学键有(填“共价键”或“离子键”)_________。
(2)球形干燥管中的干燥剂可选用(至少写一种)_________,结合化学方程式解释其作用_________。
(3)制备过程中末端导管必须始终插入试管A的水中,目的是①便于观察N2的流速;②_________。
(4)制备氮化钙的操作步骤:①按图示连接好实验装置;②_________;③打开活塞K并通入N2;④点燃酒精灯,进行反应;⑤反应结束后,熄灭酒精灯,继续通N2,使装置冷却至室温;⑥拆除装置,取出产物。
(5)上述步骤中③和④_________(填“能”或“不能”)交换,理由是_________。
(6)氮气不足会影响实验制得Ca3N2的纯度。为测定氮化钙的纯度,实验结束后取一定量的固体混合物于足量水中,微热使气体完全逸出,收集到气体共6.72 L(已折算到标准状况),将该气体通入装有足量灼热CuO的硬质玻璃管中充分反应,测得硬质玻璃管中固体质量减轻6.4 g。则Ca3N2的纯度为_________(用百分数表示,保留一位小数)(注:氨气能被灼热氧化铜氧化,生成一种对环境无污染气体)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某气态氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则R的摩尔质量为___。
(2)已知CO、SO2的混合气体质量共18.4g,标准状况下休积为8.96L,则可推知该混合气体的平均相对分子质量为___。
(3)标准状况下9.03×1023个CH4所占的体积为___,与___个NH3含有相同数目的氢原子。
(4)与16gN2H4所含有分子数相同的氧气的体积(标准状况)是___L。
(5)质量比为51:28的NH3、CO所含质子数之比为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列说法正确的是
A.5.85g氯化钠所含的离子数为0.1NA
B.2.8gN2中含有共用电子对的数目为0.1NA
C.0.1molF2中含有共价键的数目为0.2NA
D.0.1molH2与Cl2的混合气体充分反应后体系中含有共价键数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2 L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示。

(1)由图中所给数据进行分析,该反应的化学方程式为 ;
(2)反应从开始至2分钟,用Z的浓度变化 表示的平均反应速率为v(Z)= ;
(3)2min反应达平衡容器内混合气体的平均相对分子质量比起始时 (填增大、减小或不变);混合气体密度比起始时 (填增大、减小或不变)。
(4)将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n (X) = n (Y) = n (Z),则原混合气体中a : b = 。
(5)下列措施能加快反应速率的是 。
A.恒压时充入He
B.恒容时充入He
C.恒容时充入X
D.及时分离出Z
E.升高温度
F.选择高效的催化剂
(6)下列说法正确的是 。
A.升高温度改变化学反应的限度
B.已知正反应是吸热反应,升高温度平衡向右移动,正反应速率加快,逆反应速率减慢
C.化学反应的限度与时间长短无关 D.化学反应的限度是不可能改变的
E. 增大Y的浓度,正反应速率加快,逆反应速率减慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个密闭容器,中间有一无摩擦、可自由滑动的隔板(厚度不计)将容器分成两部分,当左边充入8molN2,右边充入CO和CO2的混合气体共64g时,隔板处于如图位置(保持温度不变)。
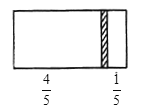
(1)右边气体的物质的量为___。
(2)右边气体中CO和CO2的质量之比为__。
(3)若改变右边CO和CO2的充入量而使隔板处于距离右端1/3处,保持温度不变,则前后两次充入情况容器内的压强之比为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值,下列说法正确的是( )
A. 常温下,4.6gNO2气体中含有的分子数为0.1NA
B. 常温常压下,22.4L SO2中含有的分子数小于NA
C. 0.1mol氯气参加反应时转移的电子数为0.2NA
D. 用含有0.1mol FeCl3的饱和溶液配制的氢氧化铁胶体中,胶体粒子数等于0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】80 ℃时,2 L密闭容器中充入0.40 mol N2O4,发生反应N2O4(g)![]() 2NO2(g) ΔH=+53 kJ/mol,获得如下数据。下列判断正确的是
2NO2(g) ΔH=+53 kJ/mol,获得如下数据。下列判断正确的是
时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
c(NO2)/mol·L-1 | 0.00 | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
A. 升高温度该反应的平衡常数K减小
B. 该反应的 ΔS <0
C. 反应达平衡时吸热15.9 kJ
D. 100 s时再通入0.40 mol N2O4,达新平衡时N2O4的体积分数减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com