
【题目】下列有关物质的性质与用途具有对应关系的是
A.硫酸铁易溶于水,可用作净水剂
B.次氯酸具有弱酸性,可用作漂白剂
C.氧化钙能与水反应,可用作食品干燥剂
D.晶体硅熔点高,可用作半导体材料
科目:高中化学 来源: 题型:
【题目】12mL浓度为0.1mol/L的Na2SO3溶液恰好与15mL浓度为0.02mol/L的HClO4溶液完全反应。已知Na2SO3被HClO4氧化为Na2SO4,则元素Cl在还原产物中的化合价为
A. -1价 B. +1价 C. +3价 D. +5价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 合成纤维与人造纤维可以统称为化学纤维
B. 酚醛树脂和聚乙烯都是热固性塑料
C. 天然橡胶的化学组成是聚异戊二烯
D. 复合材料一般有强度高、质量轻、耐高温、耐腐蚀等优异性能,其综合性质超过了单一材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于平衡体系mA(g)+nB(g) ![]() pC(g)+qD(g) ΔH<0,有下列判断,其中正确的是
pC(g)+qD(g) ΔH<0,有下列判断,其中正确的是
A. 若平衡时,A、B的转化率相等,说明反应开始时A、B的物质的量之比为m:n
B. 若温度不变,将容器的体积扩大1倍,此时A的浓度变为原来的0.6倍,则m+n<p+q
C. 若平衡体系共有气体a mol,再向其中加入b mol B,当重新达到平衡时,气体的总物质的量等于(a+b),则m+n>p+q
D. 加催化剂或增大压强,可实现图3中a→b的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如下图是常见仪器的部分结构。

(1)写出仪器名称A___________,B_________,C__________,D__________。
(2)使用前需检查是否漏水的仪器有__________。
(3)某学生用0.100 mol·L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分为如下几步:
A.移取20.00 mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管使尖嘴处充满溶液;
D.取标准KOH溶液注入碱式滴定管至0刻度以上 2~3 cm;
E.调节液面至0或0以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度。
就此实验完成填空:
①正确操作步骤的顺序是__________________________(用字母序号填写)。
②上述B步骤操作的目的是____________________________________________。
③上述A步骤操作之前,若先用待测溶液润洗锥形瓶,则滴定结果_______(填“偏高”、“偏低”或“不变”)。
④判断到达滴定终点的实验现象是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符的是
![]()
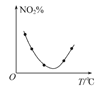
A. 图甲表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)![]() N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
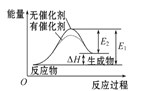
B. 图乙表示的反应是吸热反应,该图表明催化剂不能改变化学反应的焓变
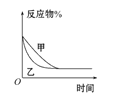
C. 图丙表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(g)的影响,则P乙>P甲
3C(g)+D(g)的影响,则P乙>P甲
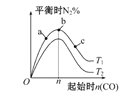
D. 图丁表示反应:4CO(g)+2NO2(g)![]() N2(g)+4CO2(g) ΔH<0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,K1>K2
N2(g)+4CO2(g) ΔH<0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,K1>K2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往蛋白质溶液里加入下列物质会产生沉淀,但再加水稀释,沉淀不会溶解的是( )
A. Na2SO4 B. NaCl C. H2SO4 D. NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在盛有足量A的体积可变的密闭容器中,加入B,发生反应:A(s)+2B(g)![]() 4C(g)+D(g);△H<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如下图。下列说法正确的是
4C(g)+D(g);△H<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如下图。下列说法正确的是
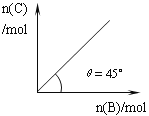
A. 若保持压强一定,当温度升高后,则图中θ>45°
B. 若再加入B,则再次达到平衡时正、逆反应速率均逐渐增大
C. 若保持压强一定,再加入B,则反应体系气体密度减小
D. 平衡时B的转化率为50%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com