
分析 (1)根据已知反应和目标反应,利用盖斯定律可知反应C3H8(g)→CH3CH=CH2(g)+H2(g)由已知的反应相减得到,则△H=△H1-△H2;
(2)负极通入丙烷,碳元素的化合价升高,电池的正极通入O2,氧元素的化合价降低,以此来书写电池总反应方程式,原电池中阴离子向负极移动;
(3)依据平衡常数概念结合平衡状态下离子浓度和同时浓度计算得到;
(4)NaHCO3溶液的pH大于8,则水解大于电离,水解生成H2CO3,电离生成CO32-.
解答 解:(1)由C3H8(g)→CH4(g)+HC≡CH(g)+H2(g)△H1=+156.6kJ•mol-1①,
CH3CH=CH2(g)→CH4(g)+HC≡CH(g)△H2=+32.4kJ•mol-1 ②,
则根据盖斯定律,反应C3H8(g)→CH3CH=CH2(g)+H2(g)可由①-②得到,
所以△H=△H1-△H2=+156.6kJ•mol-1-(+32.4kJ•mol-1)=+124.2kJ•mol-1,
故答案为:+124.2;
(2)燃料电池中,负极上燃料失电子发生氧化反应,正极上氧化剂得电子发生还原反应,负极电极反应式为C3H8-20e-+10CO32-=13CO2+4H2O,原电池中阴离子向负极移动,即CO32-移向电池的负极,
故答案为:C3H8+10CO32--20e-=13CO2+4H2O;负;
(3)常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H+)=c(HCO3-)=10-5.6mol/L;c(H2CO3)=1.5×10-5 mol•L-1.若忽略水的电离及H2CO3的第二级电离,则H2CO3的第一级电离的平衡常数K1=$\frac{c({H}^{+})•c(HC{O}_{3}^{-})}{c({H}_{2}C{O}_{3})}$=$\frac{1{0}^{-5.6}×1{0}^{-5.6}}{1.5×1{0}^{-5}}$=4.2×10-7 mol•L-1,故答案为:4.2×10-7 mol•L-1;
(4)NaHCO3溶液的pH大于8,则水解大于电离,水解生成H2CO3,电离生成CO32-,即HCO3-?CO32-+H+,HCO3-+H2O?H2CO3+OH-,所以c(H2CO3)>c(CO32-),HCO3-的水解程度大于电离程度,
故答案为:>; HCO3-?CO32-+H+、HCO3-+H2O?H2CO3+OH-,HCO3-的水解程度大于电离程度.
点评 本题考查了多个知识点,属于小综合习题,明确盖斯定律、原电池的工作原理、电离平衡常数的计算、溶液中利用电离与水解来比较离子的浓度即可解答,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 苯不能使酸性高锰酸钾溶液褪色,所以苯不能发生氧化反应 | |
| B. | 石油的主要成分是烃,石油经过分馏可制得汽油、乙烯等产品 | |
| C. | 丙烯分子中所有原子不可能在同一平面上 | |
| D. | 石油裂解的目的是为了提高轻质液体燃料的产量和质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某元素的一种核素的核内质子数为m,中子数为n,由此一定能确定该元素的近似相对原子质量为m+n | |
| B. | 短周期元素X、Y、Z,X的阳离子与Y的阴离子具有相同的电子层结构,Z的阴离子的还原性大于等电荷数Y的阴离子的还原性,那么原子序数大小是Z>X>Y | |
| C. | 第118元素在元素周期表中的位置是第七周期VIA族 | |
| D. | 碱金属单质的熔沸点和卤素单质的熔沸点都是随核电荷数的递增而升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸可刻蚀石英制艺术品 | |
| B. | 活性炭、SO2和Na2O2都具有漂白作用,且漂白的化学原理相同 | |
| C. | 石油的裂化、煤的气化、Na2FeO4杀菌消毒均属于化学变化 | |
| D. | 氢氧化铁溶胶、水玻璃、淀粉溶液、PM2.5微粒均具有丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | F | ||||
| 3 | Na | Al | Si | S | Cl | Ar |
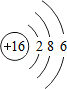 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com