
 [Cu(NH3)3]Ac·CO △H<0
[Cu(NH3)3]Ac·CO △H<0


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碱性锌锰电池性能好于普通电池的原因是能反复使用 |
| B.碱性锌锰电池的正极是MnO2,当电池中有6.5gZn反应时,将产生0.2molMnOOH |
| C.铅蓄电池放电时,负极的质量减少 |
| D.使用碱性电解质的氢氧燃料电池,负极的电极反应是H2-2e-=2H+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.锌锰碱性电池的负极材料为锌 |
| B.铅蓄电池的负极材料为铅 |
| C.镍镉电池的负极材料为镍 |
| D.锂电池的负极材料为锂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3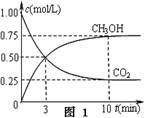
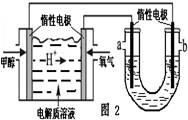
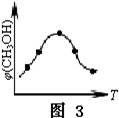
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.3 | B.4 | C.5 | D.6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 编号 | 实验内容 | 实验目的 |
| A | 取两只试管,分别加入4ml 0.01mol/L KMnO4酸性溶液,然后向一只试管中加入0.1mol/L H2C2O4溶液2ml,向另一只试管中加入0.1mol/L H2C2O4溶液4ml,记录褪色时间。 | 可以证明H2C2O4浓度越大反应速率越快。 |
| B | 向1ml 0.2mol/L NaOH溶液中滴入2滴0.1mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/L FeCl3溶液,又生成红褐色沉淀。 | 可以证明在相同温度下,溶解度Mg(OH)2>Fe(OH)3 |
| C | 测定等物质的量浓度的Na2SO3与Na2CO3溶液的pH,后者较大。 | 证明了非金属性S>C |
| D | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色会变浅。 | 可以证明Na2CO3溶液中存在水解平衡。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3OH(g) ΔH
CH3OH(g) ΔH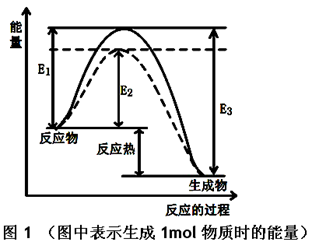

| A.2v(H2)(逆) =v(CO)(正) |
| B.混合气体的密度不变 |
| C.混合气体的平均相对分子质量不变 |
| D.CH3OH、CO、H2的浓度都不再发生变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com