
【题目】在A+B=3C+4D的反应中,下列表示该反应的化学反应速度最快的是
A.V(A)=0.5mol/(L·s)B.V(B)=0.3mol/(L·s)
C.V(C)=0.8mol/(L·s)D.V(D)=1mol/(L·s)
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】烧杯中装有50mLH2SO4和 Na2SO4 的混合液,其浓度分别为 0.16mol/L 和 2mol/L,欲使其浓度分别变为 1.6mol/L 和 0.2mol/L,在只有蒸馏水和 18mol/L 浓H2SO4以及必要仪器的条件下,完成任务:
(1)如图所示仪器,配制上述溶液不需用到的是_____(填字母).配制过程中还缺少的玻璃仪器是_____(填仪器名称)
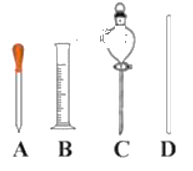
(2)下列操作可能引起所配溶液浓度偏高的有_____
A.容量瓶中原来存有少量蒸馏水
B.定容时,俯视观察刻度线
C.将量筒洗涤 2﹣3 次,并将洗涤液全部转移至容量瓶中
D.没有用蒸馏水洗烧杯 2﹣3 次,并将洗液移入容量瓶中
(3)实验操作过程中,应量取______mL18molL﹣1的浓 H 2SO4溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向1L含0.01molNaAlO2和0.02molNaOH的溶液中缓慢通入二氧化碳,随n(CO2)增大,先后发生三个不同的反应,当0.01mol<n(CO2) ![]() 0.015时发生的反应是:2 NaAlO2+ CO2+2H2O=2Al(OH)3↓+Na2CO3下列对应关系正确的是( )
0.015时发生的反应是:2 NaAlO2+ CO2+2H2O=2Al(OH)3↓+Na2CO3下列对应关系正确的是( )
选项 | n(CO2)/mol | 溶液中离子的物质的量浓度 |
A | 0 | c(Na+)>c(AlO2-)+c(OH-) |
B | 0.01 | c(Na+)>c(AlO2-)> c(OH-)>c(CO32-) |
C | 0.015 | c(Na+)> c(HCO3-)>c(CO32-)> c(OH-) |
D | 0.03 | c(Na+)> c(HCO3-)> c(OH-)>c(H+) |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中符合下列图像的是( )
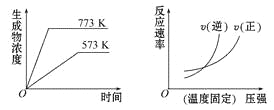
A. N2(g)+3H2(g)![]() 2NH3(g) ΔH=-Q1kJ·mol-1(Q1>0)
2NH3(g) ΔH=-Q1kJ·mol-1(Q1>0)
B. 2SO3(g)![]() 2SO2(g)+O2(g) ΔH=+Q2kJ·mol-1(Q2>0)
2SO2(g)+O2(g) ΔH=+Q2kJ·mol-1(Q2>0)
C. 4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH=-Q3kJ·mol-1(Q3>0)
4NO(g)+6H2O(g) ΔH=-Q3kJ·mol-1(Q3>0)
D. H2(g)+CO(g)![]() C(s)+H2O(g) ΔH=+Q4kJ·mol-1(Q4>0)
C(s)+H2O(g) ΔH=+Q4kJ·mol-1(Q4>0)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池,两电极一为碳棒,一为铁片,若电流表的指针发生偏转,且a极上有大量气泡生成,则以下叙述正确的是

A.a为负极,是铁片,烧杯中的溶液为硫酸
B.a为负极,是铁片,烧杯中的溶液为硫酸铜溶液
C.a为正极,是碳棒,烧杯中的溶液为硫酸
D.b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,在20 mL 0.1 mol·L-1NaOH溶液中加入0.2 mol·L-1CH3COOH溶液,所加入的溶液的体积(V)和混合液中pH变化关系的曲线如图所示,若B点的横坐标a=10,下列说法正确的是( )
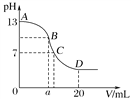
A. A~B间任意一点都满足c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
B. B点时,c(Na+)>c(CH3COO-)+c(CH3COOH)
C. C点时,c(Na+)>c(CH3COO-)>c(H+)=c(OH-)
D. A~D间任意一点都满足c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分,表中的①~⑩中元素,填空回答:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ① | ② | ③ | ④ | ||||
三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
用元素符号或化学式回答下列问题:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为______________。
(2)氧化性最强的单质是_____________。
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是_____________,碱性最强的是_____________,呈两性的氢氧化物是_____________。
(4)写出①②③⑦对应的氢化物的稳定性由强到弱的是_____________,
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前国外硝酸厂进行尾气治理普遍采用的一种方法是在有催化剂的条件下将NOx转变为N2和H2O。某组同学拟验证NO能被氨气还原并测算其转化率。
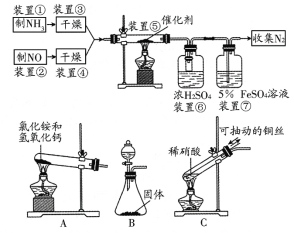
请回答下列问题:
(1)若制取氨气用A装置,则发生反应的化学方程式为_____;若制取氨气用B装置,则分液漏斗和锥形瓶中盛放的药品分别是_____、_____;
(2)用C装置制取NO时用可抽动的铜丝,其优点是_____;其反应的离子方程式为_____;
(3)装置⑦的作用可能是_____;
(4)若进入装置⑤的NO896mL(标准状况下),氨气过量,最后收集到标况下672mLN2,则NO的转化率为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO: MgSO4(s)+CO(g) ![]() MgO(s)+CO2(g)+SO2(g) △H >0,该反应在某密闭容器中达到平衡。下列分析正确的是
MgO(s)+CO2(g)+SO2(g) △H >0,该反应在某密闭容器中达到平衡。下列分析正确的是
A. 恒温恒容时,充入CO气体,达到新平衡时![]() 增大
增大
B. 容积不变时,升高温度,混合气体的平均相对分子质量减小
C. 恒温恒容时,分离出部分SO2气体可提高MgSO4的转化率
D. 恒温时,增大压强平衡逆向移动,平衡常数减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com