
分析 先根据n=$\frac{m}{M}$计算出1.7g氨气的物质的量,结合氨气分子式得出含有H原子的物质的量,然后根据N=nNA计算出含有的H的原子数;氨气分子中含有10个电子,结合氨气的物质的量计算出含有电子的物质的量.
解答 解:1.7gNH3的物质的量为:n(NH3)=$\frac{1.7g}{17g/mol}$=0.1mol,0.1mol氨气分子中含有H原子的物质的量为:0.1mol×3=0.3mol,则含有H原子的原子数约为:6.02×1023×0.3=1.806×1023;
0.1mol氨气分子中含有电子的物质的量为:0.1mol×10=1mol,
故答案为:1.806×1023;1mol.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、阿伏伽德罗常数之间的关系为解答关键,试题侧重基础知识的考查,培养了学生的化学计算能力.


 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 将氧化铝粉末溶于水 | |
| B. | 将氧化铝粉末溶于盐酸,再滴入氢氧化钠溶液 | |
| C. | 将氧化铝粉末溶于氢氧化钠溶液,再滴加氨水 | |
| D. | 将氧化铝粉末溶于盐酸,再滴入过量的氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用葡萄酿制葡萄酒 | |
| B. | 夏季油脂变质 | |
| C. | 烹鱼时加入少量的料酒和食醋可减少腥味,增加香味 | |
| D. | 用新制氢氧化铜悬浊液检验病人是否患糖尿病 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. | 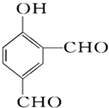 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 17g氨气中所含原子数为NA | |
| B. | 2NA个二氧化碳分子的质量为44g | |
| C. | 2.4g金属镁与足量盐酸完全反应,失电子总数为0.2NA | |
| D. | 0.1mol/LNaCl溶液中,Na+与Cl-离子总数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验用品 | 溶液温度 | 中和热 | |||
| t1 | t2 | △H | |||
| ① | 50mL0.55mol•L-1NaOH | 50mL.0.5mol•L-1HCl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol•L-1NaOH | 50mL.0.5mol•L-1HCl | 20℃ | 23.5℃ | |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
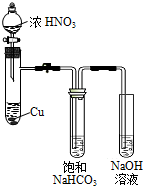 某化学学习小组发现在碱性溶液中,NO2会发生如下反应:
某化学学习小组发现在碱性溶液中,NO2会发生如下反应:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相对原子质量逐渐增大 | B. | 原子核外电子排布呈现周期性变化 | ||
| C. | 核电荷数逐渐增大 | D. | 元素的化合价呈现周期性变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com