
【题目】下列是同周期元素基态原子的最外层电子排布式,所表示的原子最容易得到电子的是( )
A. ns2 B. ns2np1 C. ns2np4 D. ns2np5
 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
【题目】“温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。
(1)下列措施中,有利于降低大气中CO2浓度的有________(填字母)。
a.减少化石燃料的使用
b.植树造林,增大植被面积
c.采用节能技术
d.利用太阳能、风能
(2)将CO2转化成有机物可有效实现碳循环。CO2转化成有机物的例子很多,如:
a.6CO2+6H2O![]() C6H12O6+6O2
C6H12O6+6O2
b.CO2+3H2![]() CH3OH+H2O
CH3OH+H2O
c.CO2+CH4![]() CH3COOH
CH3COOH
d.2CO2+6H2![]() CH2=CH2+4H2O
CH2=CH2+4H2O
以上反应中,最节能的是____________,原子利用率最高的是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
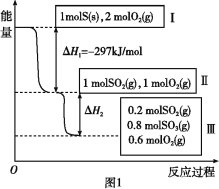
【题目】恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示。
已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6 kJ/mol。
2SO3(g) ΔH=-196.6 kJ/mol。
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式: 。
(2)状态II到状态III放出的热量为 。
(3)恒温恒容时,1 mol SO2和2 mol O2充分反应,放出热量的数值比∣ΔH2∣ (填“大”、“小”或“相等”)。
(4)将Ⅲ中的混合气体通入足量的NaOH溶液中消耗NaOH的物质的量为 ,若溶液中发生了氧化还原反应,则该过程的离子方程式为: 。
(5)恒容条件下,下列措施中能使n(SO3)/ n(SO2)增大的有 。
A.升高温度
B.充入He气
C.再充入1 mol SO2(g)和1 mol O2(g)
D.使用催化剂
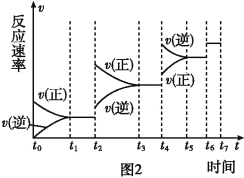
(6)某SO2(g)和O2 (g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是 ;图中表示平衡混合物中SO3的含量最高的一段时间是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重金属元素铬的毒性较大,含铬废水需经处理达标后才能排放。
I.某工业废水中主要含有Cr3+,同时还含有少量的Fe3+、Al3+、Ca2+和Mg2+等,且酸性较强。为回收利用,通常采用如下流程处理:
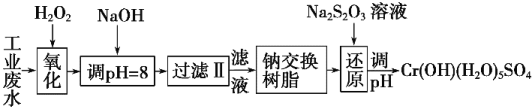
注:部分阳离子常温下以氢氧化物形式完全沉淀时溶液的pH见下表。
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
pH | 3.7 | 9.6 | 11.1 | 8 | 9(>9溶解)[ |
(1)氧化过程中可代替H2O2的最佳试剂是 (填序号)。
A.Na2O2 B.FeCl3 C.KMnO4
(2)加入NaOH溶液调整溶液pH=8时,除去的离子是 (填序号);已知钠离子交换树脂的原理:Mn++nNaR―→MRn+nNa+,此步操作被交换除去的杂质离子是 (填序号)。
A.Fe3+ B.Al3+ C.Ca2+ D.Mg2+
II.酸性条件下,六价铬主要以Cr2O72-形式存在,工业上常用电解法处理含Cr2O72-的废水:该法用Fe作电极电解含Cr2O72-的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。
(3)电解时能否用Cu电极来代替Fe电极? (填“能”或“不能”),理由是: 。
(4)电解时阳极附近溶液中Cr2O72-转化为Cr3+的离子方程式为: 。
(5)常温下,Cr(OH)3的溶度积Ksp=1×10-32,当溶液中的c(Cr3+)=10-5 mol·L-1时,pH= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】充分燃烧2.8g某有机物A,生成8.8g CO2和3.6g H2O,这种有机物蒸气的相对密度是 相同条件下N2的2倍.
(1)求该有机物的分子式 .
(2)该有机物链状同分异构体的结构简式为: 、 、 .
(3)若有机物A在核磁共振氢谱中只有一个信号峰(即只有一种氢原子),则用键线式表示的结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列现象或事实不能用同一原理解释的是( )
A.浓硝酸和硝酸银用棕色试剂瓶保存
B.常温下铁和铂都不溶于浓硝酸
C.亚硫酸盐和硫酸亚铁固体长期暴露在空气中变质
D.H2O2溶液中加入少量MnO2或FeCl3溶液都能增大反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅被誉为无机非金属材料的主角。有科学家提出硅是“21世纪的能源”“未来的石油”。下列有关说法正确的是( )
A.硅的含量居第二位,在地球上有丰富的单质硅资源,如石英、水晶的主要成分都是SiO2
B.单质硅是一种良好的半导体材料,可用于制造太阳能电池
C.存放NaOH溶液的试剂瓶应用玻璃塞
D.60gSiO2含有1NA 个SiO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的相对分子质量为102。
(1)经测定,该有机物含碳、氢、氧三种元素,其中含氢的质量分数为9.8%,分子中氢原子个数为氧原子的5倍。该有机物的分子式是________;若该有机物无甲基、无醚键,且能发生银镜反应,则该有机物的官能团的名称_______________,写出该有机物与新制的氢氧化铜的反应的化学方程式:________________________________________________。
(2)经红外光谱测定,该有机物分子中含有一个羧基、一个羟基和一个碳碳双键,则其可能的结构简式为_____________________________________________________(提示:羟基不能连在碳碳双键上)。
(3)经测定,该有机物只含碳、氢两种元素,且所有原子均在同一平面,请写出该有机物的结构简式:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物CxHmOn完全燃烧时需要氧气的物质的量是该有机物的x倍,则其化学式中x、m、n的关系不可能的是 ( )
A.m︰n=2︰1 B.m=2x+2 C.x︰m︰n=1︰2︰1 D.m>2x+2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com