
元素周期表中某区域的一些元素多用于制造半导体材料,它们是 ( )
A.左、下方区域的金属元素 B.右、上方区域的非金属元素
C.过渡元素中 D.金属元素与非金属元素分界线附近的元素
科目:高中化学 来源: 题型:
将3.48 g四氧化三铁完全溶解在100 mL 1 mol·L-1的硫酸中,然后加入K2Cr2O7溶液
25 mL,恰好使溶液中的Fe2+全部转化为Fe3+,Cr2O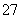 全部转化为Cr3+,则K2Cr2O7溶液的物质的量浓度是 ( )
全部转化为Cr3+,则K2Cr2O7溶液的物质的量浓度是 ( )
A.0.05 mol·L-1 B.0.1 mol·L-1
C.0.2 mol·L-1 D.0.3 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA 为阿伏加德罗常数的值。下列说法正确的是[微软用户7]
A.0.1molN2与足量的H2反应,转移的电子数是0.6NA
B.常温下, 0.1 mol·L-1 NH4NO3溶液中含有的氮原子数是0.2NA
C.常温常压下,3.2 g O2和3.2 g O3所含氧原子数都是0.2NA
D.2.24 L CO和CO2的混合气体中所含的碳原子数为0.1 N A
查看答案和解析>>
科目:高中化学 来源: 题型:
已知x、Y是元素周期表中前20号元素,二者原子序数相差3,x、Y能形成化台物M,下列说法正确的是
A.若X和Y处于同一周期,则X的原子半径肯定小于Y的原子半径
B.若X和Y处于不同的周期,则M溶于水所得溶液肯定呈碱性
C.若M属于离子化合物,则该化合物中只存在离子键
D若M属于共价化台物,则该分子中原子个数比可能为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨工业上常用下列方法制备H2 :
方法: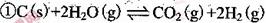
方法: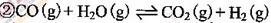
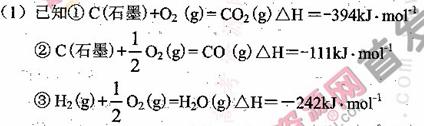
试计算25℃时由方法②制备l000g H2所放出的能量为_________ kJ。
(2)在一定的条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器,发生反应:
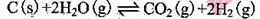 其相关数据如下表所示:
其相关数据如下表所示:
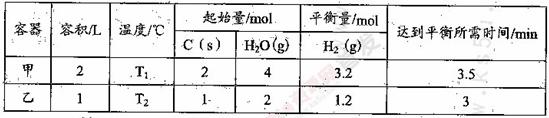
①T1_________T2 (填“>”、“=”或“<”);
T1℃时,该反应的平衡常数K=_________ 。
②乙容器中,当反应进行到1.5min时,H2O(g)的物质的量浓度范围是_________。
③一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是_________。
A.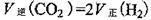
B混合气体的密度保持不变
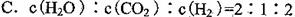
D.混合气体的平均相对分子质量保持不变
④某同学为了研究反应条件对化学平衡的影响,测得逆反应速率与时间的关系如图所示:
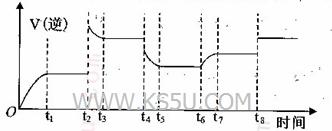
可见在t1、t3、t5、t7时反应都达了到平衡状态,如果t2、t4、t6、t8时都只改变了一个反应条件,则从t1到t8哪个时间段H2O (g)的平衡转化率最低_________,t4时刻改变的条件是__________。
⑤在25 ℃时,c mol/L,的醋酸与0.02mol/L NaOH溶液等体积混合后溶液刚好呈中性,
用含c的代数式表示CH3COOH的电离常数Ka=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
镍氢电池的总反应式是H2+2NiO(OH) 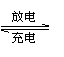 2Ni(OH)2,根据此反应式判断,此电池放电时,负极上发生反应的物质是( )。
2Ni(OH)2,根据此反应式判断,此电池放电时,负极上发生反应的物质是( )。
A.NiO(OH) B.Ni(OH)2 C.H2 D.H2和NiO(OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应既属于氧化还原反应,又属于吸热反应的是 ( )
A.铝片与稀盐酸反应 B.灼热的炭与二氧化碳反应
C.甲烷在氧气中燃烧 D.Ba(OH)2·8H2O与NH4Cl反应
查看答案和解析>>
科目:高中化学 来源: 题型:
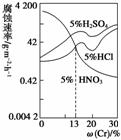 如图是三种稀酸对FeCr合金随Cr含量变化的腐蚀性实验结果,
如图是三种稀酸对FeCr合金随Cr含量变化的腐蚀性实验结果,
下列有关说法正确的是 ( )
A.稀硝酸对FeCr合金的腐蚀性比稀硫酸和稀盐酸的弱
B.稀硝酸和铁反应的化学方程式是Fe+6HNO3(稀)===Fe(NO3)3
+3NO2↑+3H2O
C.Cr含量大于13%时,因为三种酸中硫酸的氢离子浓度最大,
所以对FeCr合金的腐蚀性最强
D.随着Cr含量增加,稀硝酸对FeCr合金的腐蚀性减弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com