
业已发现许多含金的化合物可以治疗风湿症等疾病,引起科学家广泛兴趣。在吡啶(![]() )的衍生物2,2'-联吡啶(代号A)中加入冰醋酸与30% H2O2的混合溶液,反应完成后加入数倍体积的丙酮,析出白色针状晶体B(分子式C10H8N2O2)。B的红外光谱显示它有一种A没有的化学键。B分成两份,一份与HAuCl4在温热的甲醇中反应得到深黄色沉淀C。另一份在热水中与NaAuCl4反应,得到亮黄色粉末D。用银量法测得C不含游离氯而D含游离氯7.18%。C的紫外光谱在211nm处有吸收峰,与B的213nm特征吸收峰相近,而D则没有这一吸收。C和D中金的配位数都是4。
)的衍生物2,2'-联吡啶(代号A)中加入冰醋酸与30% H2O2的混合溶液,反应完成后加入数倍体积的丙酮,析出白色针状晶体B(分子式C10H8N2O2)。B的红外光谱显示它有一种A没有的化学键。B分成两份,一份与HAuCl4在温热的甲醇中反应得到深黄色沉淀C。另一份在热水中与NaAuCl4反应,得到亮黄色粉末D。用银量法测得C不含游离氯而D含游离氯7.18%。C的紫外光谱在211nm处有吸收峰,与B的213nm特征吸收峰相近,而D则没有这一吸收。C和D中金的配位数都是4。
5-1 画出A、B、C、D的结构式。
5-2 在制备B的过程中加入丙酮起什么作用?
5-3 给出用游离氯测定值得出D的化学式的推理和计算的过程。科目:高中化学 来源: 题型:
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ④ | ⑦ | ⑨ | |||
| 4 | ② | ⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
| 原子半径 *10-10 m |
1.52 | 1.11 | 0.70 | 0.66 | 1.86 | 1.60 | 1.11 | 1.04 | 0.99 |
| 最高正价最低负价 | +1 | +2 | +5 -3 |
-2 |
+1 | +2 | +5 -3 |
+6 -2 |
+7 -1 |
| 族 周期 |
IA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ||||||||
| 3 | ||||||||


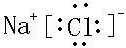
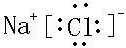
查看答案和解析>>
科目:高中化学 来源: 题型:
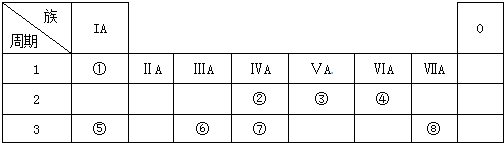
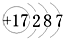
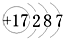
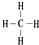

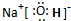
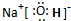
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 |
ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑨ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |


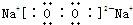
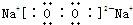


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com