
 Fe(OH)2+2Ni(OH)2下列推断中不正确的是( )
Fe(OH)2+2Ni(OH)2下列推断中不正确的是( )| A. | ① | B. | ①②④ | C. | ①③④ | D. | ②③④ |
分析 ①放电时为原电池,负极发生氧化反应,正极发生还原反应;
②充电时为电解质,阴极发生还原反应;
③充电时为电解质,阳极发生氧化反应;
④Fe(OH)2、2Ni(OH)2只能存在于碱性溶液中,在酸性条件下不能存在.
解答 解:①放电时为原电池,负极发生氧化反应,正极发生还原反应,反应中Fe失去电子,为负极,Ni2O3获得电子,为正极,故①错误;
②充电时为电解质,阴极发生还原反应,Fe(OH)2在阴极获得电子,阴极上的电极反应式是Fe(OH)2+2e-═Fe+2OH-,故②正确;
③充电时为电解质,阳极发生氧化反应,Ni(OH)2发生氧化反应,为阳极,故③正确;
④Fe(OH)2、2Ni(OH)2只能存在于碱性溶液中,在酸性条件下不能存在,故电解质溶液必须是碱性溶液,故④正确,
故选:A.
点评 本题以二次电池为载体考查原电池与电解池的工作原理,注意根据总反应式从氧化还原的角度判断原电池的正负极与电解池的阴阳极.


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:解答题
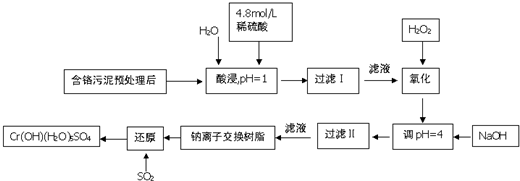
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | 7.0 | - | - | - |
| 沉淀完全是的pH | 3.7 | 9.0 | 11.1 | 8 | 9(>9溶解) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解稀硫酸制H2、O2时铜作阳极 | B. | 用电解法精炼粗铜时粗铜作阴极 | ||
| C. | 在镀件上电镀铜时用金属铜作阴极 | D. | 铜锌原电池中铜是正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用Cu作阴、阳电极,电解CuCl2溶液 | |
| B. | 用Cu作阴、阳电极,电解K2SO4溶液 | |
| C. | 铜锌合金在潮湿空气中发生电化学腐蚀 | |
| D. | Cu作原电池的负极,碳棒作正极,NaCl溶液作电解质溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸 | B. | NaCl | C. | AgNO3 | D. | KNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 冰醋酸、纯碱、芒硝、生石灰分别属于酸、碱、盐、氧化物 | |
| B. | HClO、H2SO4(浓)、HNO3均具有强氧化性,都是氧化性酸 | |
| C. | 漂白粉、福尔马林、冰水、王水、氯水均为混合物 | |
| D. | Na2O、NaOH、Na2CO3、NaCl都属于钠的含氧化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2LCCl4中含有C-Cl键的数目为2NA | |
| B. | NA个D2O分子中,含有10NA个电子 | |
| C. | 117克氯化钠固体中,含有2NA个氯化钠分子 | |
| D. | 32克SO2与足量的O2反应转移的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①③④ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com