
【题目】甲醇是重要的化工原料,又可称为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g)![]() CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g)![]() CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
回答下列问题:
(1)反应①的化学平衡常数K的表达式为___;图1中能正确反映平衡常数K随温度变化关系的曲线为___(填曲线标记字母),其判断理由是___。
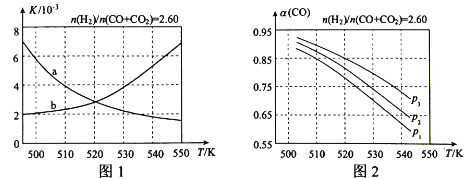
(2)合成气的组成![]() =2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。α(CO)值随温度升高而___(填“增大”或“减小”),其原因是___。图2中的压强由大到小为___,其判断理由是___。
=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。α(CO)值随温度升高而___(填“增大”或“减小”),其原因是___。图2中的压强由大到小为___,其判断理由是___。
【答案】K=![]() a 反应①为放热反应,平衡常数应随温度升高变小 减小 升高温度时,反应①为放热反应,平衡向向左移动,使得体系中CO的量增大;反应③为吸热反应,平衡向右移动,又产生CO的量增大;总结果,随温度升高,使CO的转化率降低 P3>P2>P1 相同温度下,由于反应①为气体分子数减小的反应,加压有利于提升CO的转化率;而反应③为气体分子数不变的反应,产生CO的量不受压强影响,故增大压强时,有利于CO的转化率升高
a 反应①为放热反应,平衡常数应随温度升高变小 减小 升高温度时,反应①为放热反应,平衡向向左移动,使得体系中CO的量增大;反应③为吸热反应,平衡向右移动,又产生CO的量增大;总结果,随温度升高,使CO的转化率降低 P3>P2>P1 相同温度下,由于反应①为气体分子数减小的反应,加压有利于提升CO的转化率;而反应③为气体分子数不变的反应,产生CO的量不受压强影响,故增大压强时,有利于CO的转化率升高
【解析】
(1)平衡常数为生成物浓度幂之积与反应物浓度幂之积的比值;反应①为放热反应,温度升高,K值减小;
(2)由图象可知,压强一定时,温度越高,CO的转化率降低,根据升高温度对反应①和③的影响进行分析;相同温度下,反应③为等体积反应,压强改变不影响平衡的移动,反应①正向为体积缩小的反应,增大压强,平衡正向移动,CO转化率增大,据此进行分析判断。
(1)反应①的化学平衡常数K=![]() ;反应①为放热反应,温度升高,K值减小,因此能正确反映平衡常数K随温度变化关系的曲线为a;
;反应①为放热反应,温度升高,K值减小,因此能正确反映平衡常数K随温度变化关系的曲线为a;
(2)由图象可知,压强一定时,温度越高,CO的转化率降低,反应①为放热反应,升高温度平衡逆向移动,体系中CO的量争夺,反应③为吸热反应,升高温度,平衡正向移动,CO的量增多,因此随着温度的升高,CO的转化率减小;相同温度下,反应③为等体积反应,压强改变不影响平衡的移动,反应①正向为体积缩小的反应,增大压强,平衡正向移动,CO转化率增大,因此增大压强有利于CO的转化率的升高,所以压强的大小关系为:P3>P2>P1。


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
【题目】某工厂排放出有毒物质NOCl,它遇水就会生成NO3-,NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为______。水源中的NO3-对人类健康会产生危害。为了降低水源中NO3-的浓度,有研究人员建议在碱性条件下用铝粉将NO3-还原为N2,该反应的离子方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将煤直接作为燃料燃烧,不但热效率较低,且产生烟尘、二氧化硫、氮氧化物等物质,造成严重的环境污染。煤的干馏是提高煤的利用率、生产重要化工原料、绣像污染物排放量的有效措施之一。某化学学习小组在实验室条件下探究煤干馏的现象及产物,装置如图所示,请回答有关问题:

(1)煤干馏的条件是___。
(2)盛有冷水的烧杯的作用是___。
(3)实验后检验有粗氨水生成的操作是___。
(4)已知CO不能使溴水退色,若将从具支试管支管口处逸出的气体通入溴水中,发现溴水退色,则说明煤的干馏产生了___。
(5)从煤焦油中分离出苯、甲苯、二甲苯的实验方法是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料。回答下列问题:
对于反应2SiHCl3(g)=SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323K和343K时SiHCl3的转化率随时间变化的结果如图所示。
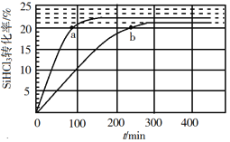
在343K下:要提高SiHCl3转化率,可采取的措施是___;要缩短反应达到平衡的时间,可采取的措施有___、___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是( )
A.18gT2O(3H2O)中,含有的电子总数为10NA
B.5.6g铁与足量的水蒸气在高温条件下反应,转移电子数是0.3NA
C.标准状况下,4.48LCH3Cl中所含原子总数为NA
D.1molSO2与2molO2在一定条件下充分反应,生成SO3的分子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙苯催化脱氢制苯乙烯反应:![]() +H2(g)。
+H2(g)。
工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1︰9),控制反应温度600℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)示意图如图:
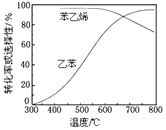
①掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实___。
②控制反应温度为600℃的理由是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应3A(g)+B(g)![]() 4C(g)达平衡的是( )
4C(g)达平衡的是( )
A.单位时间内消耗amolB,同时生成3amolA
B.容器内压强不再变化
C.混合气体的总物质的量不再发生变化
D.3v(A)=v(B)=4v(C)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验:利用如图装置可以验证元素的非金属性的变化规律。
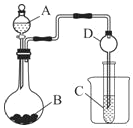
(1)图中:A装置名称是___,干燥管D的作用是___。
(2)实验室中现有药品Na2S、KMnO4、MnO2、浓盐酸,请从中选择合适药品设计实验验证氯的非金属性大于硫,烧瓶中发生反应的离子方程式为___。
(3)若要用此装置证明酸性:HNO3>H2CO3>H2SiO3,进而证明非金属性:N>C>Si,从以下所给物质中选出甲同学设计的实验所用到物质:
①稀HNO3溶液 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2
装置A、C中所选试剂分别为__(填序号);能说明酸性H2CO3>H2SiO3的实验现象是__。
(二)四种短周期元素W、X、Y、Z,原子序数依次增大,请回答下列问题。
W | X | Y | Z | |
结构或性质 | 最高价氧化物对应的水化物与其气态氢化物反应得到离子化合物 | 焰色反应 呈黄色 | 在同周期主族元素形成的简单离子中,离子半径最小,它的最高价氧化物为两性氧化物 | 最高正价与最低负价之和为零 |
(1)Z在元素周期表中位于___族。
(2)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其他三种物质发生化学反应,该元素是___(填元素符号)。
(3)①下列可作为比较X和Y金属性强弱的依据是___(填序号)。
a.自然界中的含量
b.单质与酸反应时失去的电子数
c.单质与水反应的难易程度
d.最高价氧化物对应水化物的碱性
②从原子结构的角度解释X的金属性强于Y的原因:___。
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似。体积和浓度均相等的HW3与X的最高价氧化物对应的水化物混合,反应的化学方程式是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 分子式为C4H8有机物最多存在4个C﹣C单键
B. ![]() 和
和![]() 均是芳香烃,
均是芳香烃,![]() 既是芳香烃又是芳香化合物
既是芳香烃又是芳香化合物
C. ![]() 和
和![]() 分子组成相差一个﹣CH2﹣,因此是同系物关系
分子组成相差一个﹣CH2﹣,因此是同系物关系
D. 分子式为C2H6O的红外光谱图上发现有C﹣H键和C﹣O键的振动吸收,由此可以初步推测有机物结构简式为C2H5﹣OH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com