
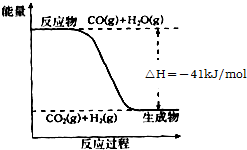
 研究化学反应中的能量变化有重要意义.请根据学过知识回答下列问题:
研究化学反应中的能量变化有重要意义.请根据学过知识回答下列问题:分析 (1)根据图象分析反应是放热反应,焓变为-41KJ/mol,然后根据热化学方程式的书写方法写出,最后根据盖斯定律计算得到所需的化学方程式;
(2)反应的焓变△H=反应物键能总和-生成物键能总和计算.
解答 解:(1)由图象分析反应是放热反应,焓变为-41KJ/mol,热化学方程式为:CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41kJ•mol-1,①
C(s)+H2O(g)═CO(g)+H2(g)△H=+135kJ•mol-1 ②
依据盖斯定律②-①得到:C(s)+CO2(g)═2CO(g)△H=+176kJ•mol-1,
故答案为:C(s)+CO2(g)═2CO(g)△H=+176kJ•mol-1;
(2)N≡N键的键能是948.9kJ•mol-1,H-H键的键能是436.0kJ•mol-1,N-H键的键能是391.55kJ•mol-1.则$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)═NH3(g);
△H=反应物键能总和-生成物键能总和=$\frac{1}{2}$×948.9kJ•mol-1 +$\frac{3}{2}$×436.0kJ•mol-1 -3×391.55kJ•mol-1=-46.2kJ/mol;
故答案为:-46.2kJ/mol.
点评 本题考查了热化学方程式书写方法和注意问题,注意键能计算焓变的方法,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,10mL0.02 mol•L-1 HCl溶液与10mL0.02 mol•L-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=11 | |
| B. | 在0.1 mol•L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+) | |
| C. | 中和物质的量浓度与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 | |
| D. | 配制三氯化铁溶液时应将三氯化铁溶于浓盐酸,再加水稀释至所需浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、OH一、HCO3- Cu2+ | B. | NH4+、NO3-、OH-、K+ | ||
| C. | H+、K+、CO32-、SO42- | D. | Ba2+、OH一、C1-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2S+CuSO4═H2SO4+CuS↓ | B. | H2SO4+CuO═CuSO4+H2O | ||
| C. | 2NaOH+CO2═Na2CO3+H2O | D. | Fe2O3+3CO═2Fe+3CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 25 | T2 |
| 水的离子积常数 | 1×10-14 | 1×10-12 |
| 难溶物 | Fe(OH)2 | Fe(OH)3 | Zn(OH)2 |
| Ksp | 8.0×10-16 | 8.0×10-38 | 1.0×10-17 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所得溶液的质量分数:w=36.5c/1000 | |
| B. | 36.5 gHCl气体在标准状况下占有的体积约为22.4L | |
| C. | 所得溶液的物质的量浓度:c=1 mol•L-1 | |
| D. | 所得溶液中含有NA个HCl分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| A.c (CH3COO-)>c (Na+)>c (H+)>c (OH-) | B.c (CH3COO-)>c (Na+)>c (OH-)>c (H+) |
| C.c (CH3COO-)>c (H+)>c (Na+)>c (OH-) | D.c (Na+)>c(CH3COO-)>c (OH-)>c (H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com