
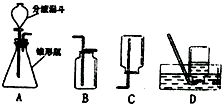
 过氧化氢溶液在二氧化锰作催化剂的条件下能迅速分解,分液漏斗可以通过调节活塞控制液体的滴加速度,请根据图回答以下问题:
过氧化氢溶液在二氧化锰作催化剂的条件下能迅速分解,分液漏斗可以通过调节活塞控制液体的滴加速度,请根据图回答以下问题:分析 (1)依据过氧化氢、二氧化锰状态分析解答;
(2)过氧化氢在二氧化锰催化剂条件下反应生成水和氧气;氧气难溶于水,要收集一瓶纯净的氧气,可以用排水法收集;
(3)装置漏气会造成收集不到气体.
解答 解:(1)过氧化氢为液体,应盛放着分液漏斗中,二氧化锰为固体,应盛放着锥形瓶中;
故答案为:过氧化氢溶液;二氧化锰;
(2)氧化氢在二氧化锰催化剂条件下反应生成水和氧气,用该方法制取氧气的化学反应文字表达式:过氧化氢→水+氧气;氧气难溶于水,要收集一瓶纯净的氧气,可以用排水法收集;
故答案为:过氧化氢→水+氧气;D;
(3)某同学观察到锥形瓶内有大量气泡时,开始用B装置收集氧气,过一段时间后用带火星的木条伸入瓶口、瓶中和瓶底,都末见木条复燃.其原因可能是装置的气密性不好,漏气,
故答案为:装置的气密性不好.
点评 本题考查了氧气的实验室制备方法,明确制备原理及常见仪器的使用方法和注意事项是解题关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
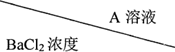 | 0.2mol/L | 0.1mol/L | 0.02mol/L |
| 0.2mol/L | 浑浊 | 浑浊 | 少许浑浊 |
| 0.1mol/L | 浑浊 | 少许浑浊 | 无现象 |
| 0.02mol/L | 少许浑浊 | 无现象 | 无现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用加入适量铜粉的方法除去Cu(NO3)2溶液中混有的AgNO3 | |
| B. | 用洗气瓶中的NaOH溶液除去CO2中混有的HCl气体 | |
| C. | 向某无色未知溶液中仅加入BaCl2溶液,以检验未知溶液的SO42- | |
| D. | 先后添加酚酞试液、BaCl2溶液,将盐酸、硫酸、硫酸钠、氢氧化钠和硝酸钾五种无色溶液鉴别开 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
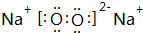 ,该氧化物与水反应的离子方程式2Na2O2+2H2O=4Na++4OH-+O2↑.
,该氧化物与水反应的离子方程式2Na2O2+2H2O=4Na++4OH-+O2↑.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com