
| 元素代号 | X | Y | Z | W |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | -2 |
| A. | X、Y分别与W形成的化合物都具有两性 | |
| B. | Z、W在同一主族 | |
| C. | 气态氢化物的稳定性为H2W<H2Z | |
| D. | X和Y对应的氢氧化物的碱性强弱比较:X(OH)2<Y(OH)3 |
分析 元素的最高正价=最外层电子数,最高正价和最低负价绝对值的和为8,Z、W两元素最外层电子数为6,故为第ⅥA元素,而Z的半径大于W,故在周期表中W元素在上面,Z在下面,W为没有最高正价的O,Z为S,Y元素最最外层电子数为3,为B或Al,但是半径比氧和硫均大,故位于氧元素和硫元素的中间,应为Al,X的半径比铝大,最外层电子数为2,应为Mg,以此解答该题.
解答 解:元素的最高正价=最外层电子数,最高正价和最低负价绝对值的和为8,Z、W两元素最外层电子数为6,故为第ⅥA元素,而Z的半径大于W,故在周期表中W元素在上面,Z在下面,W为没有最高正价的O,Z为S,Y元素最最外层电子数为3,为B或Al,但是半径比氧和硫均大,故位于氧元素和硫元素的中间,应为Al,X的半径比铝大,最外层电子数为2,应为Mg,
A.氧化镁不具有两性,故A错误;
B.Z为S,W为O,为第ⅥA元素,故B正确;
C.非金属性S<O,元素的非金属性越强,对应的氢化物越稳定,故C错误;
D.金属性Mg>Al,元素的金属性越强,对应的氢氧化物的碱性越强,故D错误.
故选B.
点评 本题考查元素的性质,学生能利用原子半径及化合价来推断出元素是解答本题的关键,并熟悉元素及其单质、化合物的性质来解答即可,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 向蛋白质溶液中滴加饱和Na2SO4溶液或浓硝酸均会产生白色沉淀,是因为蛋白质变性 | |
| B. | 提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤、干燥的方法 | |
| C. | 某钾盐溶于盐酸,产生无色无味气体,通过澄清石灰水,石灰水变浑浊,该钾盐一定是K2CO3 | |
| D. | 进行K与水反应的实验操作:可在培养皿中放些水,然后取绿豆大小的钾,用滤纸吸干表面的煤油,投入培养皿中 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚氯乙烯的单体是CH2=CHCl | |
| B. | 通过加聚反应得到的聚乙烯属于天然高分子化合物 | |
| C. | 聚乙烯的链节是CH2=CH2 | |
| D. | 聚乙烯的产量是衡量一个国家石油化工发展水平的标志 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴苯(溴):加入四氯化碳,振荡、静置、分液 | |
| B. | 乙醇(水):加入生石灰,蒸馏 | |
| C. | 乙酸乙酯(乙酸):加入氢氧化钠溶液,静置、分液 | |
| D. | 乙烯(乙烷):通过酸性高锰酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
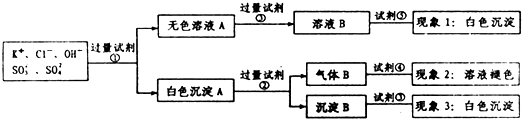
| A. | 试剂③是AgNO3溶液,试剂⑤是HNO3,现象1中白色沉淀是AgCl | |
| B. | 现象3中白色沉淀是BaSO4 | |
| C. | 试剂②是盐酸,试剂③是硝酸 | |
| D. | 产生现象2的离子方程式是:Br2+2H2O+SO2═4H++2Br-+SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 30 | B. | 20 | C. | 12 | D. | 17 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
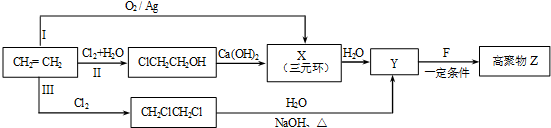
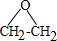 .
.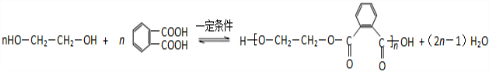 .
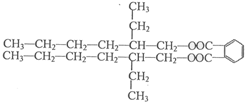
.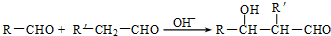 (R、R'代表烃基或氢原子).合成P的路线如下图所示.D分子中有8个碳原子,其主链上有6个碳原子,且分子内只含有两个-CH3.
(R、R'代表烃基或氢原子).合成P的路线如下图所示.D分子中有8个碳原子,其主链上有6个碳原子,且分子内只含有两个-CH3.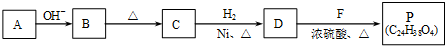
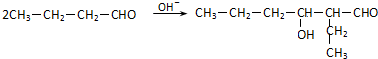 .
.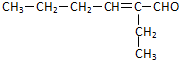 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的电了式: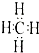 | B. | 乙炔的结构简式:CHCH | ||
| C. | 硫离子的结构示意图: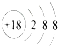 | D. | 中子数为10的原子:${\;}_{8}^{10}$O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com