
下列有关实验操作、现象和解释(或结论)都正确的是( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| B | AgI沉淀中滴入稀KCl溶液 | 有白色沉淀出现 | AgCl比AgI更难溶 |
| C | Al箔插入稀HNO3中 | 无现象 | Al箔表面被HNO3氧化,形成致密的氧化膜 |
| D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
|
| A. | A | B. | B | C. | C | D. | D |
| 化学实验方案的评价;难溶电解质的溶解平衡及沉淀转化的本质;二价Fe离子和三价Fe离子的检验;铝金属及其化合物的性质实验;氨的制取和性质. | |
| 专题: | 实验评价题. |
| 分析: | A.铁过量,反应生成硝酸亚铁; B.AgI的溶解度比AgCl的小; C.Al与稀硝酸发生氧化还原反应生成NO; D.浓氨水中存在NH3.H2O⇌NH4++OH﹣,碱遇红色石蕊试纸变蓝. |
| 解答: | 解:A.过量的Fe粉中加入稀HNO3,反应生成硝酸亚铁,滴入KSCN溶液,溶液不显红色,故A错误; B.AgI的溶解度比AgCl的小,则AgI沉淀中滴入稀KCl溶液,不会生成白色沉淀,故B错误; C.Al与稀硝酸发生氧化还原反应生成NO、硝酸铝和水,观察到气泡冒出,故C错误; D.浓氨水中存在NH3.H2O⇌NH4++OH﹣,碱遇红色石蕊试纸变蓝,则说明浓氨水呈碱性,故D正确; 故选D. |
| 点评: | 本题考查化学实验方案的评价,明确发生的化学反应是解答本题的关键,注意发生的反应与实验现象的关系,选项B为易错点,题目难度中等. |


科目:高中化学 来源: 题型:
观察下列各物质间的转化图,仔细分析后回答各题。
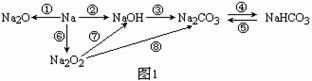
(1)图1中属于氧化还原反应的有_______个,试书写呼吸面具或潜水艇供氧剂分别与H2O和CO2反应的化学方程式: _______________; ______________
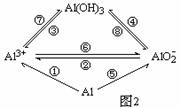
(2)若实现图2中①②③④各反应的转化,可加入相同的试剂,其化学式为_________;试写出反应②的离子方程式:______________________________
若实现图2中⑤⑥⑧各转化反应,可加入相同的试剂,其化学式为__________;
氢氧化铝的用途很多,试写出实验室用反应⑦制取氢氧化铝的离子方程式:
_______________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关电解原理的说法正确的是( )
①电解是把电能转变成化学能;
②电解是把化学能转变为电能;
③电解质溶液的导电是化学变化,金属的导电是物理变化;
④不能自发进行的氧化还原反应,通过电解原理可以实现;
⑤任何溶液被电解时必然会导致氧化还原反应的发生
A.①②③④ B.②③⑤
C.③④ D.①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素( )
|
| A. | 在自然界中只以化合态的形式存在 | B. | 单质常用作半导体材料和光导纤维 |
|
| C. | 最高价氧化物不与酸反应 | D. | 气态氢化物比甲烷稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学用语表示不正确的是 ( )
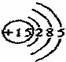 A.P原子的结构示意图:
A.P原子的结构示意图:
B.NaCl的电子式为: 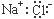
C.HCN分子的结构式:H—C≡N
D.含78个中子的碘的放射性核素: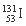
查看答案和解析>>
科目:高中化学 来源: 题型:
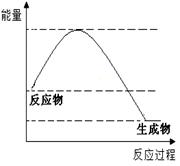
某反应的反应过程和能量变化如图所示,下列有关该反应的叙述
正确的是( )
A. 该反应是吸热反应
B. 反应物的总能量低于生成物的总能量
C. 该反应的反应热△H < 0
D. 加入催化剂后反应放出的热会减少
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在指定溶液中关于离子共存的说法正确的是( )
|
| A. | 25℃时溶液中一定大量共存:Na+、Ca2+、Cl﹣、SO42﹣ |
|
| B. | 能与铝反应放出氢气的溶液中一定共存:Mg2+、Cu2+、SO42﹣、NO3﹣ |
|
| C. | 弱碱性溶液中可能大量共存:Na+、K+、Cl‾、HCO3‾ |
|
| D. | 0.1mol/LFeCl3溶液中可能大量共存:Fe2+、NH4+、SCN﹣、SO42﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
I.铝是地壳中含量最高的金属元素,其单质及其合金在生产生活中的应用十分广泛。
(1)金属铝的生产是以Al2O3为原料,与冰晶石(Na3A1F6)在熔融状态下进行电解,其阴极电极反应式为 ,其电极均由石墨材料做成,则电解时不断消耗的电极是 (填“阴极”或“阳极”),冰晶石的作用为 。
(2)铝电池性能优越,A1-Ag2O电池可用作水下动力电源,化学反应为2Al+3Ag2O+2NaOH=2NaAlO2+6Ag+H2O,则负极的电极反应式为 ,正极附近溶液的pH (填“变大”“不变”或“变小”)。
已知:①2Al(s)+3Cl2(g)=2AlCl3(s) △H1=-1390 .8kJ/mol
②4Al(s)+3O2(g)=2Al2O3(s) △H2=-3339.6kJ/mol
③2C(s)+O2(g)=2CO(g) △H3=-221.0kJ/mol
Al2O3(s)+ 3C(s)+3Cl2(g)=2AlCl3(s)+3CO(g)的△H= 。
Ⅱ.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)下图是在一定温度和压强下N2和H2反应生成1 mol NH3过程中的能量变化示意图,
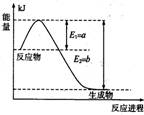
请写出合成氨的热化学反应方程式: (ΔH的数值用含字母a、b的代数式表示)。
(2)工业合成氨的反应为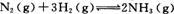 在一定温度下,
在一定温度下,
将一定量的N2和H2通入到体积为1 L的密闭容器中,反应达到平衡后,改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是 。
A.增大压强 B.增大反应物的浓度 C.使用催化剂 D.降低温度
Ⅲ.铁及其化合物在生活、生产中有广泛应用。请回答下列问题。
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2 6SO2+Fe3O4,有3 m01FeS2参加反应,转移 mol电子。
6SO2+Fe3O4,有3 m01FeS2参加反应,转移 mol电子。
(2)氯化铁溶液称为化学试剂中的“多面手”,写出SO2通入氯化铁溶液中反应的离子方程式: 。
Ⅳ.锰及其化合物应用越来越广泛,MnO2是一种重要的无机功能材料,制备Mn02的方法之一是以石墨为电极,电解酸化的MnSO4溶液,阳极的电极反应式为 。现以铅蓄电池为电源电解酸化的MnS04溶液,如图所示
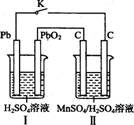
铅蓄电池的总反应方程式为 ,当蓄电池中有4 mol H+被消耗时,则电路中通过的电子的物质的量为 ,MnO2的理论产量为 g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com