
【题目】化工生产要遵守三大原则:充分利用原料、充分利用能量、保护环境。下列描述不符合以上原则的是
A. 煅烧硫铁矿时使用沸腾炉 B. 制盐酸时通入过量氯气使氢气反应完全
C. 制硫酸时使用热交换器 D. 氨碱法生产中循环使用氨气和二氧化碳
科目:高中化学 来源: 题型:
【题目】能与Al反应生成H2的透明溶液中可能大量共存的一组离子是( )
A. K+、NO3-、AlO2-、Na+ B. NH4+、SO42-、CO32-、NO3-
C. Mg2+、Fe3+、Cl-、SCN- D. K+、Ca2+、Cl-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有2.8g有机物A,完全燃烧生成0.15mol CO2 和1.8g H2O,A的质谱图如下图示:

已知:![]()
(X为卤原子,M为烃基或含酯基的取代基等),由有机物A合成G(香豆素)的步骤如下:

回答下列问题:
(1)写出A和银氨溶液反应的化学方程式_________
(2)D的结构简式为____________
(3)二氢香豆素(![]() )常用作香豆素的替代品,鉴别二氢香豆素和它的一种同分异构体(
)常用作香豆素的替代品,鉴别二氢香豆素和它的一种同分异构体(![]() )需要用到的试剂有:NaOH溶液、_______、________.
)需要用到的试剂有:NaOH溶液、_______、________.
(4)F有多种同分异构体,写出同时满足下列条件的两种同分异构体的结构简式:______.
Ⅰ.分子中除苯环外,无其它环状结构;
Ⅱ.苯环上有两个处于对位的取代基;
Ⅲ.能发生水解反应,不能与Na反应;
Ⅳ.能与新制Cu(OH)2按物质的量比1:2发生氧化反应
(5)又知:![]() (R,R′为烃基),试写出以苯和丙烯(CH2=CH-CH3)为原料,合成
(R,R′为烃基),试写出以苯和丙烯(CH2=CH-CH3)为原料,合成![]() 的路线流程图如下:
的路线流程图如下:
![]()
步骤①的反应条件和试剂______,步骤②的反应类型_____,P的结构简式_________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别由短周期元素m、n、p、q组成的单质依次为甲、乙、丙、丁,有关反应关系如图所示(部分产物省略)。其中甲为黄绿色气体,M、N均为10电子分子且M的水溶液呈碱性,Q为离子化合物,下列说法中正确的是

A. 原子半径的大小m>q>n>p
B. 元素非金属性q>n>p
C. Q的溶液可以保存在细口玻璃试剂瓶
D. n的氧化物的水化物一定为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1.12 g铁粉加到25 mL 2 mol/L的氯化铁溶液中,完全反应后,其结果是
A. 铁有剩余,溶液呈浅绿色,c(Cl-)基本不变
B. 往溶液中滴加无色KSCN溶液,未显红色
C. 溶液中n(Fe2+)与n(Fe3+)之比为6∶1
D. 氧化产物与还原产物的物质的量之比为2∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁被称为“国防金属”,镁及其合金用途很广,目前世界上60%的镁从海水中提取。从海水中提取镁的流程如下:
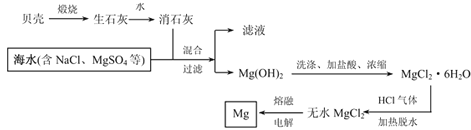
请根据上述流程图和镁及化合物的性质回答下列问题:
(1)用贝壳煅烧生石灰的反应方程式:________________
(2)氢氧化镁溶于盐酸的离子方程式为:_____________。
(3)简述,由MgCl2·6H2O制无水MgCl2,加热时通HCl气体的主要原因是:___________。
(4)金属镁属于(填写下列编号):___________。
a.黑色金属 b.有色金属 c.轻金属 d.重金属 e.贵金属
(5)Mg(OH)2煅烧可得熔点很高的MgO,MgO的电子式为:____________。
(6)MgCl2和AlCl3的熔点均较低,加MgO和Al2O3的熔点都很高。为什么冶炼金属镁是电解MgCl2,而冶炼金属铝则电解Al2O3:_______________。
(7)某MgCl2溶液的浓度为0.01mol/L,在该溶液中滴加NaOH溶液至pH=10,此时溶液中的Mg2+是否沉淀完全?_________(填“是”或“否”),此时c(Mg2+)=_________。
(已知:Ksp[Mg(OH)2]=1.8×10-11)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com