
【题目】原子序数依次增大的四种元素A、B、C、D分别处于第1~4周期,其中A原子核是一个质子;B原子核外电子有6种不同的运动状态,B与C可形成正四面体形分子,D原子外围电子排布为3d104s1。请回答下列问题:
(1)这四种元素中电负性最大的是____(填元素符号,下同),第一电离能最小的是____;
(2)C所在的主族元素气态氢化物中,沸点最低的是____(填化学式);
(3)B元素可形成多种单质,其中”只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体结构如图所示,其原子的杂化类型为______;
(4)D的醋酸盐晶体局部结构如图,该晶体中含有的化学键是____(填选项序号);

①极性键 ②非极性键 ③配位键 ④金属键
(5)某学生所做的有关D元素的实验流程如下图:
D单质![]() 棕色的烟
棕色的烟![]() 绿色溶液
绿色溶液![]() 蓝色沉淀
蓝色沉淀![]() 蓝色溶液
蓝色溶液![]() 黑色沉淀
黑色沉淀
请书写第⑤步反应的离子方程式:_____________。
【答案】ClCuHClsp2①②③[Cu(NH3)4]2++H2S+2H2O====CuS↓+2NH4++2NH3·H2O
【解析】
A原子核是一个质子,即A为H,B原子核外电子有6种不同的运动状态,说明B原子核外有6个电子,即B为C,C和F或Cl形成正四面体形,因为四种元素分别位于不同周期,因此C为Cl,根据D的外围电子排布式,推出D为Cu,(1)非金属性越强,其电负性越大,四种元素中非金属性最强的是Cl,即电负性最强的元素为Cl,第一电离能最小,说明金属性越强,非金属性越弱,因此第一电离能最强的元素是Cu;(2)Cl位于第VIIA族,HF分子间存在氢键,其余不含分子间氢键,即HF沸点最高,相对分子质量越大,分子晶体的沸点越高,另外三种卤族氢化物中HCl的分子量最小,即HCl沸点最低;(3)根据图示,该碳原子有3个σ键,无孤电子对,因此C的杂化类型为sp2;(4)由结构图可知该醋酸铜晶体中含有极性键、非极性键和配位键,故①②③正确;(5)分析实验流程图可知:Cu与Cl2反应生成CuCl2,蓝色沉淀为Cu(OH)2,蓝色溶液为[Cu(NH3)4]Cl2,黑色沉淀则为CuS。据此可写出离子方程式为: [Cu(NH3)4]2++H2S+2H2O====CuS↓+2NH4++2NH3·H2O


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某液态烃和溴水发生加成反应生成 2,3-二溴-2-甲基丁烷,则该烃是( )
A.3-甲基-1-丁烯B.2-甲基-2-丁烯
C.2-甲基-1-丁烯D.1-甲基-2-丁烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常以烃的含氧衍生物X为主要原料生产可降解塑料PCL{HO(CH2)5COOH}及阻燃剂四溴双酚A。合成线路如下图所示:
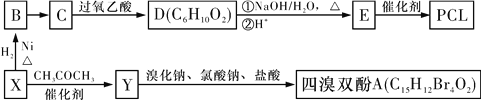
已知:①X的蒸气密度是相同条件下H2的47倍,遇FeCl3溶液显紫色;C为O。
②ROH![]() RBrOHBr。
RBrOHBr。
③RCOCH2R′![]() RCOOCH2R′。
RCOOCH2R′。
(1)X的分子式为____________;B的名称是__________。
(2)B→C还需要的反应试剂及条件是________________________。C→D的反应类型是______________。
(3)写出X→Y的化学方程式: _______________________________________。
(4)0.5 mol四溴双酚A在常温下与足量的Na2CO3溶液反应,最多消耗________mol Na2CO3。
(5)符合以下条件的C的同分异构体有__________种(不考虑立体异构)。
①含有两个甲基 ②含有一个碳碳双键 ③能发生银镜反应
(6)已知由烯烃直接制备不饱和酯的新方法为:2CH3CHCH2+2ROH+2CO+O2![]() 2CH3CHCHCOOR+2H2O,利用乙烯为有机原料(无机物和反应条件自选)合成聚合物涂料CHCH2COOCH2CH3,写出合成该涂料的反应流程图。_________________
2CH3CHCHCOOR+2H2O,利用乙烯为有机原料(无机物和反应条件自选)合成聚合物涂料CHCH2COOCH2CH3,写出合成该涂料的反应流程图。_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某“化学鸡尾酒”通过模拟臭虫散发的聚集信息素可高效诱捕臭虫,其中一种组分T可通过下列反应路线合成(部分反应条件略)。
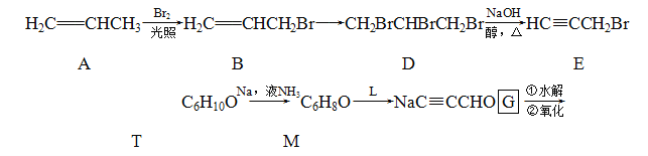
(1)A的化学名称是________,A→B新生成的官能团是________。
(2)D的核磁共振氢谱显示峰的组数为________。
(3)D→E的化学方程式为_______________________________________________。
(4)G与新制的Cu(OH)2发生反应,所得有机物的结构简式为________。
(5)L可由B与H2发生加成反应而得,已知R1CH2Br+NaC≡CR2―→R1CH2C≡CR2+NaBr,则M的结构简式为__。
(6)已知 ,则T的结构简式为________。
,则T的结构简式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组同学利用如图装置研究氨气的性质。

请回答下列问题。
(1)实验室用熟石灰与氯化铵制备氨气的化学方程式是_______。
(2)下列物质能用于干燥氨气的有_____________(填字母序号)。
a. ![]() 固体 b.
固体 b. ![]() 固体
固体
c.碱石灰 d.浓![]()
(3)B中观察到的现象是_________,反应的化学方程式是_________。
(4)C中观察到的现象是__________,反应的化学方程式是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属及其化合物在人类生活、生产中发挥着重要的作用。
(1)下列物质中不属于合金的是_______。
A.钢 B.青铜 C.黄铜 D.水银
(2)在钠、铝、铁三种金属元素中,所形成的氧化物中适宜做耐火材料的是_______,向盛有硫酸铝溶液的试管中滴加足量氨水,反应的离子方程式是_____________。
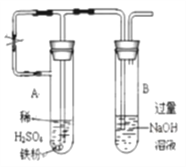
(3)乙同学为了获得持久白色的Fe(OH)2沉淀,准备用右图所示装置,用不含O2的蒸馏水配制的NaOH溶液与新制的FeSO4溶液反应。获得不含O2的蒸馏水的方法是_______。反应开始时,打开止水夹;一段时间后,关闭止水夹,在试管_______(填“A”或“B”)中观察到白色的Fe(OH)2。
(4)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是____________。
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
(5)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。请写出FeCl3溶液与铜反应的离子方程式:__________;
(6)某研究性学习小组内测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:①取少量待测溶液,滴入KSCN溶液呈红色,该现象说明该溶液中含有的离子是_______;②验证该溶液中含有Fe2+,正确的实验方法是_______;A.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+B.取适量溶液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中含有Fe2+C.观察溶液是否呈浅绿色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像正确的是
A. 向氢氧化钙和氢氧化钠混合溶液中通入二氧化碳
B. 用氢氧化钠溶液滴定等浓度的盐酸和醋酸
C. 向氢氧化钠溶液中通入二氧化碳
D. 氯化氢和氯气的混合气体通入氢氧化钠溶液中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com