
| A、28g N2中含有氮原子数为nA |
| B、1molNa与足量O2反应转移的电子数为nA |
| C、常温常压下,22.4LCO2中含有的分子数为nA |
| D、1mol?L-1K2SO4溶液中含有的钾离子数为nA |
| m |
| M |
| m |
| M |
| 28g |
| 28g/mol |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、物质的量浓度相等的溶液pH关系:pH(NaClO)>pH(Na2CO3)>pH(CH3COONa) |
| B、向NaClO溶液中通少量CO2:CO2+NaClO+H2O→NaHCO3+HClO |
| C、a mol/L HClO与b mol/L NaOH溶液等体积混合后所得溶液中c(Na+)>c(ClO-),则a一定小于b |
| D、向氯水中加入NaHCO3固体,可以增大氯水中次氯酸的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 叙述I | 叙述II |
| A | 二氧化硅有导电性 | 二氧化硅可用于制备光导纤维 |
| B | 次氯酸有强氧化性 | 次氯酸可以使有色布条褪色 |
| C | Fe3+具有氧化性 | 可以用KSCN溶液检验的Fe 3+存在 |
| D | Na2O、Na2O2组成元素相同 | 与二氧化碳反应产物也相同 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同温同压下,相同体积的物质,其物质的量一定相等 |
| B、不同的外界条件下,等物质的量的甲烷和一氧化碳所含的分子数不一定相等 |
| C、14g一氧化碳气体一定比20 g氧气的体积小 |
| D、相同条件下的一氧化碳气体和氮气,若体积相等,则分子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使甲基橙变红色的溶液中:NO3-、SO42-、Fe2+、Na+ |
| B、澄清透明的溶液中:ClO-、MnO4-、Al3+、SO42- |
| C、澄清透明的溶液中:MnO4-、Al3+、SO42-、K+ |
| D、水电离产生c(H+)=1×10-12mol/L的溶液中,Mg2+、Na+、Cl-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.7 g羟基所含电子的数目为NA |
| B、0.1 mol丙烯醛中含有双键的数目为O.1NA |
| C、室温时,pH=13的1.0 L Ba(OH)2溶液中含有OH-的数目为0.2NA |
| D、标准状况下,7.8 g苯中含氢原子的数目为O.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化钡溶液和稀硫酸反应:Ba2++SO42-=BaSO4↓ |
| B、浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑ |
| C、SO2通入溴水中:SO2+Br2+2H2O=SO42-+2Br-+4H+ |
| D、钠放于水中:Na+2H2O=Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
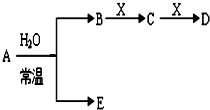 已知如图是常见元素形成的单质或化合物A、B、C、D、E、X转化关系(部分生成物和反应条件略去)
已知如图是常见元素形成的单质或化合物A、B、C、D、E、X转化关系(部分生成物和反应条件略去)查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com