

| A. | a口放出气体为N2 | |
| B. | 电池总反应的产物与甲醇燃烧产物一样 | |
| C. | 用该电池电解精制铜,当消耗1mol甲醇时,可溶解粗铜中3mol铜 | |
| D. | 质子将由C1电极区经交换膜向C2电极区运动 |
分析 A、燃料电池的正极上是氧气的电子的还原反应;
B、燃料电池总反应是燃料燃烧的化学方程式;
C、根据电解池、燃料电池的电极反应式结合电子守恒进行计算即可;
D、在原电池中,阳离子从负极移向正极.
解答 解:A、该装置是燃料电池,通入燃料的电极是负极,通入空气的电极是正极,正极上是氧气的电子的还原反应,空气中的氧气得电子,所以剩余是氮气,即a口放出气体为N2,故A正确;
B、燃料电池总反应是燃料燃烧的化学方程式,在酸性介质下,甲醇燃料电池的总反应产物与甲醇燃烧产物一样,故B正确;
C、燃料电池总反应是:2CH4O+3O2=2CO2+4H2O,当消耗1mol甲醇时,转移电子是6mol,用该电池电解精制铜,可根据主反应:Cu-2e-=Cu2+,转移电子是6mol,溶解粗铜中3mol铜,但是阳极上先是活泼金属失电子,然后是金属铜失电子,所以当消耗1mol甲醇时,可溶解粗铜中铜的量小于3mol,故C错误;
D、该装置是燃料电池,通入燃料的电极是负极,通入空气的电极是正极,阳离子从负极移向正极,由C1电极区经交换膜向C2电极区运动,故D正确.
故选C.
点评 本题考查学生燃料电池的工作原理以及电极反应式的有关计算等知识,属于综合知识的考查,难度中等.


科目:高中化学 来源: 题型:解答题
 ;
;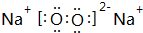 ;
;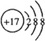 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M、N不可能在同一周期 | B. | M一定在N的下一周期 | ||
| C. | MN2肯定是共价化合物 | D. | M、N可能在同一主族 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
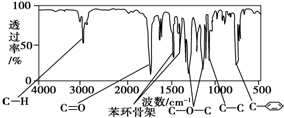 化合物A经李比希法测得其 中含C 72.0%、H 6.67%,其余含有氧;质谱法分析得知A的相对分子质量为150.现代仪器分析有机化合物的分子结构有以下两种方法.
化合物A经李比希法测得其 中含C 72.0%、H 6.67%,其余含有氧;质谱法分析得知A的相对分子质量为150.现代仪器分析有机化合物的分子结构有以下两种方法.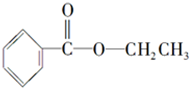 、
、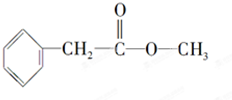 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 将1molNH4NO3溶于一定浓度的稀氨水中,溶液呈中性,若不考虑挥发,溶液中含有的NH4+数目小于NA | |
| B. | 24g石墨烯(单层石墨)中含有六元环的个数为NA | |
| C. | 标准状况下,6.72LNO2与足量水反应转移电子数目为0.2NA | |
| D. | 4.6gC2H6O加入足量的金属钠,充分作用,生成H2分子数一定为0.05NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
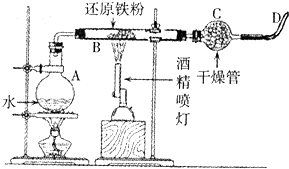 铁是人类使用最广泛的金属.
铁是人类使用最广泛的金属.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
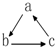 (“→”表示一步完成)关系相互转化的是( )
(“→”表示一步完成)关系相互转化的是( )| 选项 | A | B | C | D |
| a | Fe | H2SO4 | Al(OH)3 | HNO3 |
| b | FeCl3 | SO2 | Na[Al(OH)4] | NO |
| c | FeCl2 | SO3 | Al2O3 | NO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com