
| A. | Na0H固体在空气中变质 | B. | 钢铁生锈 | ||
| C. | 物质的燃烧 | D. | 植物的光合作用 |
分析 根据发生的化学反应中是否存在元素的化合价变化,存在元素的化合价升降的反应为氧化还原反应,以此来解答.
解答 解:A.Na0H固体在空气中变质,发生Na0H与二氧化碳反应生成碳酸钠和水,没有化合价的变化,与氧化还原反应无关,故A选;
B.钢铁的生锈发生Fe、氧气、水的反应生成氧化铁,有元素的化合价升降,与氧化还原反应有关,故B不选;
C.燃料的燃烧为氧化还原反应,如甲烷、氢气的燃烧,与氧化还原反应有关,故C不选;
D.植物的光合作用,将二氧化碳吸收放出氧气,有元素的化合价升降,与氧化还原反应有关,故D不选;
故选A.
点评 本题以生活中的化学反应考查氧化还原反应,明确发生的化学反应及元素的化合价变化是解答本题的关键,题目难度不大.


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol NO的质量是30g | |
| B. | 标准状况下,1 mol H2O的体积是22.4 L | |
| C. | 17 g NH3含有的氢原子总数为6.02×1023 | |
| D. | 0.1 mol Na2CO3中,Na+的物质的量为 0.1 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
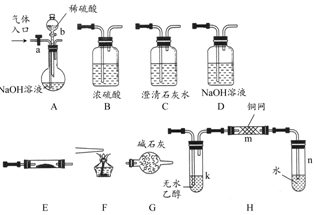 如图所示为常见气体制备、分离、干燥和性质验证的部分仪器装置(加热设备及夹持固定装置均略去),请根据要求完成下列各题(仪器装置可任意选用,必要时可重复选择).
如图所示为常见气体制备、分离、干燥和性质验证的部分仪器装置(加热设备及夹持固定装置均略去),请根据要求完成下列各题(仪器装置可任意选用,必要时可重复选择).查看答案和解析>>
科目:高中化学 来源: 题型:实验题
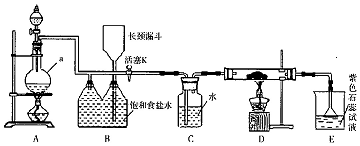
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①② | B. | 只有②④ | C. | 只有②③④ | D. | 只有①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
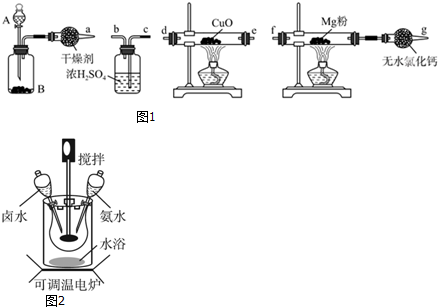
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:实验题
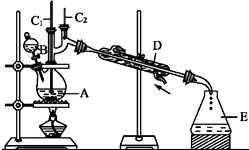
| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.810 9 | 微溶 |
| 正丁醛 | 75.7 | 0.801 7 | 微溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com