
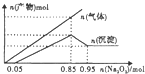
| A. | 混合溶液中m(Al3+)为5.4g | B. | 混合溶液中c(Mg2+)为0.5mol/L | ||
| C. | 混合溶液的pH=2 | D. | 混合溶液中c(Cl-)为1.7mol/L |
分析 HCl、AlCl3、MgCl2的混合溶液中加入过氧化钠,会将铝离子、镁离子沉淀,得到的沉淀是氢氧化铝和氢氧化镁的混合物,根据氢氧化铝溶解消耗的氢氧化钠的量结合元素守恒,可以计算含有的铝离子的质量,根据开始阶段,盐酸和氢氧化钠中和消耗的氢氧化钠的量来计算盐酸的pH,根据将离子完全沉淀消耗的氢氧化钠的量计算含有的镁离子的量,据电荷守恒计算溶液中氯离子的浓度即可.
解答 解:A、氢氧化铝溶解,消耗过氧化钠的物质的量是0.1mol,即消耗的氢氧化钠的物质的量是0.2mol,根据Al(OH)3~OH-,所以氢氧化铝的物质的量是0.2mol,根据Al元素守恒,则铝离子的质量是0.2mol×27g/mol=5.4g,故A正确;
B、根据Al3+~3OH-,所以沉淀铝离子消耗0.6mol氢氧化钠,即0.3mol过氧化钠,根据图示,将镁离子沉淀则消耗0.5mol过氧化钠,即1.0mol氢氧化钠,根据Mg2+~2OH-,所以镁离子的物质的量是0.5mol,浓度是0.5mol/L,故B正确;
C、开始阶段,盐酸和氢氧化钠中和消耗的过氧化钠的物质的量是0.05mol,即消耗氢氧化钠的物质的量是0.1mol,所以盐酸氢离子物质的量是0.1mol,浓度是0.1mol/L,pH=1,故C错误;
D、在溶液中,铝离子的物质的量浓度是0.2mol/L,氢离子浓度是0.1mol/L,镁离子的物质的量浓度是0.5mol/L,根据电荷守恒:3c(Al3+)+2c(Mg2+)+c(H+)=c(Cl-),得到溶液中c(Cl-)为1.7mol/L,故D正确.
故选C.
点评 对于图象分析题的解题规律:要明确每一段图象发生的化学反应、知道拐点代表的含义及溶液中溶质的成分,结合方程式对有关问题进行分析.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol甲苯含C-H键的数目为6NA | |
| B. | 反应5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O中生成28gN2时,转移电子数目为15NA | |
| C. | 1molFeCl3与水反应完全转化为氢氧化铁胶体后,胶体粒子的数目为NA | |
| D. | 含有4.6g钠元素的过氧化钠和氧化钠的混合物中,所含离子总数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
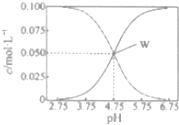 25℃时,有c(CH2COOH)+c(CH2COO-)=0.1mol•L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH2COOH)、c(CH2COO-)与pH的关系如图所示.下列有关溶液中离子浓度关系的叙述不正确的是( )
25℃时,有c(CH2COOH)+c(CH2COO-)=0.1mol•L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH2COOH)、c(CH2COO-)与pH的关系如图所示.下列有关溶液中离子浓度关系的叙述不正确的是( )| A. | 25℃时,醋酸的电离常数Ka=1×10-4.75 | |
| B. | W点所表示的溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH-) | |
| C. | pH=5.5的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | pH=3.5的溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子式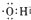 可以表示烃基,也可以表示氢氧根离子 可以表示烃基,也可以表示氢氧根离子 | |
| B. | 磷原子的简化电子排布式:[He]3s23p3 | |
| C. | 聚丙烯链节的结构简式为:-CH2-CH-CH2- | |
| D. | 用惰性电极电解MgCl2溶液的离子方程式为:Mg2++2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+Mg(OH)2↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中,Na+、Fe3+、NO3-、Cl-可能大量共存 | |
| B. | 和溴水反应的离子方程式:Br2+SO32-+H2O=2H++2Br-+SO42- | |
| C. | 和Ba(OH)2溶液加热反应的离子方程式:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 1L0.1mol•L-1该溶液和足量的硝酸充分反应,生成2.24L(标准状况)SO2气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
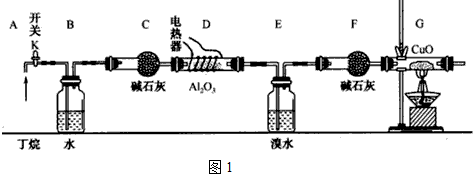
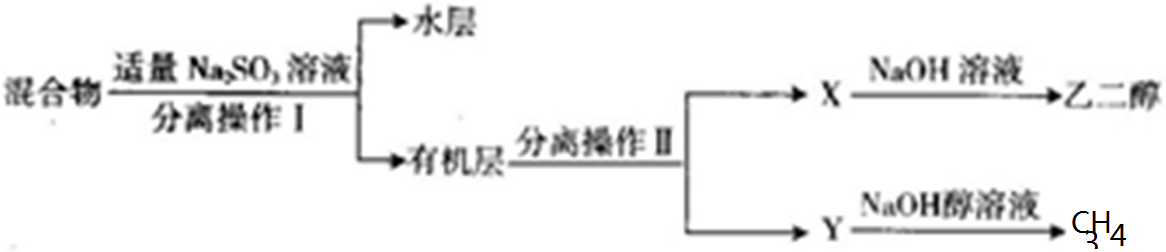
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯可作为水果的催熟剂 | |
| B. | 地沟油经过处理,可用来制造肥皂 | |
| C. | 漂白粉长期暴露在空气中会变质失效 | |
| D. | 煤炭燃烧过程安装固硫装置,可有效提高煤的利用率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
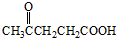 )合成聚芳酯E的路线:
)合成聚芳酯E的路线:
 +SOCl2→
+SOCl2→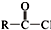 +SO2+HCl
+SO2+HCl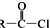 +R′OH→
+R′OH→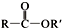 +HCl(R、R′表示烃基)
+HCl(R、R′表示烃基) .
. .
.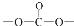 结构;
结构; .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com