
�밴Ҫ��ش��������⣺
(1)��֪25 ��ʱ��Ksp[Mg(OH)2]��1.8��10��11��Ksp[Cu(OH)2]��2.2��10��20����25 ���£���Ũ�Ⱦ�Ϊ0.1 mol��L��1��MgCl2��CuCl2�����Һ����μ��백ˮ��������________����(�ѧʽ)�����ɸó��������ӷ���ʽΪ____________________________��
(2)25 ��ʱ����0.01 mol��L��1��MgCl2��Һ�У���μ���ŨNaOH��Һ���պó��ֳ���ʱ����Һ��pHΪ________����Mg2����ȫ����ʱ����Һ��pHΪ________(������Һ����仯����֪lg 2.4��0.4��lg 7.7��0.9)��
(3)��֪25 ��ʱ��Ksp(AgCl)��1.8��10��10����AgCl��������ˮ���γɱ�����Һ����Һ�е�c(Ag��)ԼΪ______ mol��L��1��
(4)��֪25 ��ʱ��Ksp[Fe(OH)3]��2.79��10��39�����¶��·�ӦFe(OH)3��3H��Fe3����3H2O��ƽ�ⳣ��K��________��
������(1)��ΪKsp[Cu(OH)2]<Ksp[Mg(OH)2]������������Cu(OH)2������(2)Ksp[Mg(OH)2]��1.8��10��11��c(Mg2��)��c2(OH��)��0.01��c2(OH��)����c(OH��)��4.2��10��5 mol��L��1��c(H��)��KW/c(OH��)��2.4��10��10 mol��L��1����pH��9.6������pH��9.6ʱ����ʼ����Mg(OH)2������һ����Ϊ��������Һ�е�����Ũ��С��1��10��5 mol��L��1ʱ�������Ѿ���ȫ����Mg2����ȫ����ʱ�У�1��10��5��
c2(OH��)��1.8��10��11����c(OH��)��1.3��10��3 mol��L��1����ʱ��c(H��)��7.7��10��12 mol��L��1��pH��11.1��(3)Ksp(AgCl)��1.8��10��10��c(Ag��)��c(Cl��)��c2(Ag��)����ã�c(Ag��)��1.3��10��5 mol��L��1��(4)Ksp[Fe(OH)3]��c(Fe3��)��c3(OH��)����ʾ��Ӧ��ƽ�ⳣ��ΪK��c(Fe3��)/c3(H��)��25 ��ʱˮ�����ӻ�ΪKW��c(H��)��c(OH��)��1��
10��14���Ƶ�K��Ksp[Fe(OH)3]/K ����K��2.79��10��39/(1��10��14)3��2.79��103��
����K��2.79��10��39/(1��10��14)3��2.79��103��
�𰸡�(1)Cu(OH)2��Cu2����2NH3��H2O===Cu(OH)2����2NH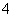 ��(2)9.6��11.1��(3)1.3��10��5��(4)2.79��103
��(2)9.6��11.1��(3)1.3��10��5��(4)2.79��103


 ��ĩ��ϰ���ϵ�д�
��ĩ��ϰ���ϵ�д� ����ѧ�䵥Ԫ������ĩר����100��ϵ�д�
����ѧ�䵥Ԫ������ĩר����100��ϵ�д� �Ƹ�360�ȶ����ܾ�ϵ�д�
�Ƹ�360�ȶ����ܾ�ϵ�д� ���⿼����Ԫ���Ծ�ϵ�д�
���⿼����Ԫ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���й���ú��ʯ�͡���Ȼ������Դ��˵����ȷ���� (����)��
A��ú��ʯ�͡���Ȼ����Ϊ��������Դ
B��ʯ�Ͳ�Ʒ�������ھۺϷ�Ӧ
C����Ȼ������������Ҫ�ɷֶ��Ǽ���
D��ˮú����ͨ��ú��Һ���õ�������ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ��ͨ����ԭ�����͵�������ȵķ��ӻ����ӳ�Ϊ�ȵ����壬���Ƿ��ֵȵ������Ľṹ����������(���ȵ���ԭ��)��B3N3H6����Ϊ���������뱽�ǵȵ����壬������˵���в���ȷ����(����)
A������������ֻ���м��Լ�
B�������ܷ����ӳɷ�Ӧ��ȡ����Ӧ
C�������Ķ���ȡ������3��ͬ���칹��
D����������ʹKMnO4������Һ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪ij��Һ��ֻ����OH����H����NH ��Cl���������ӣ�ijͬѧ�Ʋ����Һ�и�����Ũ�ȴ�С˳��������������ֹ�ϵ��
��Cl���������ӣ�ijͬѧ�Ʋ����Һ�и�����Ũ�ȴ�С˳��������������ֹ�ϵ��
��c(Cl��)>c(NH )>c(H��)>c(OH��)
)>c(H��)>c(OH��)
��c(Cl��)>c(NH )>c(OH��)>c(H��)
)>c(OH��)>c(H��)
��c(NH )>c(Cl��)>c(OH��)>c(H��)
)>c(Cl��)>c(OH��)>c(H��)
��c(Cl��)>c(H��)>c(NH )>c(OH��)
)>c(OH��)
��д���пհף�
(1)����Һ��ֻ�ܽ���һ�����ʣ������ʵ�������________����������Ũ�ȴ�С˳���ϵ����ȷ����________(ѡ�����)��
(2)��������ϵ�Т�����ȷ�ģ�����Һ�����ʵĻ�ѧʽ��_________________����������ϵ�Т�����ȷ�ģ�����Һ�����ʵĻ�ѧʽ��________��
(3)������Һ�������ȵ�ϡ����Ͱ�ˮ��϶��ɣ���ǡ�ó����ԣ�����ǰ��������ʵ���Ũ��(����ڡ���С�ڡ����ڡ�����ͬ)________��ˮ�����ʵ���Ũ�ȣ����ǰ������c(H��)�Ͱ�ˮ��c(OH��)�Ĺ�ϵ��
c(H��)______c(OH��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��50 mL 0.018 mol��L��1��AgNO3��Һ�м���50 mL 0.02 mol
��L��1���������ɳ�������֪Ksp(AgCl)��1.8��10��10�������ɳ��������Һ��
c(Ag��)��pH�ֱ�Ϊ (����)��
A��1.8��10��7 mol��L��1,2�� B��1��10��7 mol��L��1,2
C��1.8��10��7 mol��L��1,3�� D��1��10��7 mol��L��1,3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����йغϳɰ���ҵ��˵���У���ȷ���� (����)��
A���Ӻϳ��������Ļ�������У�����ռ15%�������������Ĺ�����Ч�ʶ�
�ܵ�
B�����ڰ���Һ����N2��H2��ʵ��������ѭ��ʹ�ã�����������˵�����IJ�
�ʺܸ�
C���ϳɰ���ҵ�ķ�Ӧ�¶ȿ�����500 �棬Ŀ����ʹ��ѧƽ��������Ӧ����
�ƶ�
D���ҹ��ϳɰ������õ�ѹǿ��10��30 MPa����Ϊ��ѹǿ������ý�Ļ�����
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����������ɵ����������ϳɰ����ķ��������1918��ŵ������ѧ�����ֽ������͵�������ij�ܱ������У���һ�������·�Ӧ���й�����Ϊ��
| ��Ŀ | H2 | N2 | NH3 |
| ��ʼʱ | 5 mol��L��1 | 3 mol��L��1 | 0 |
| 2 sĩ | 2 mol��L��1 |
(1)�����͵�����Ӧ���ɰ���(��2 s��)�ķ�Ӧ����v(H2)��__________������ʱ�Ѵ�ƽ�⣬������ƽ�ⳣ��Ϊ__________��
(2)��ͼ��ʾ�ϳ�NH3��Ӧ��ʱ��t0��t6�з�Ӧ�����뷴Ӧ��������ͼ���������дﵽ��ѧƽ���ʱ����У���ѧƽ�ⳣ������һ��ʱ����__________��
��t0��t1����t2��t3����t3��t4����t5��t6
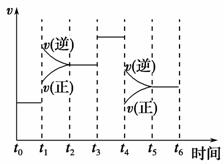
��t1ʱ�ı�������������¶ȣ���˵���ϳ�NH3��Ӧ���ʱ䦤H________0(����ڡ���С�ڡ�)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����(1100��)�����ܱ������з�����Ӧ��
Na2SO4(s)��4H2(g) Na2S(s)��4H2O(g)������˵����ȷ����
Na2S(s)��4H2O(g)������˵����ȷ����
A. �÷�Ӧ��ƽ�ⳣ������ʽK��c(H2O)/c(H2)
B. ��������������ܶȻ�ѹǿ���ֲ��䣬��˵���÷�Ӧ�Ѵﵽƽ��״̬
C. ��Na2SO4�������ı���ʼ����H2��Ũ�ȣ���ƽ��ʱH2��ת���ʲ���
D. ����ʼʱͶ��2.84gNa2SO4��һ����H2��Ӧ��ƽ��ʱ�����ڹ��干��2.264g����Na2SO4��ת����Ϊ45%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������������ʵ�Ӧ�û�������ʹ�����ǣ� ��
A��ʳ�ο�����ζ����Ҳ����ʳƷ������
B������ȼ�ջ�ʯȼ�������������������Ҫ����֮һ
C��װ�β����ͷŵļ�ȩ����ɿ�����Ⱦ
D��ĥ�����Ĵ��������ʣ�������к��ʱ���˰�����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com