
| A. | 水是还原产物 | B. | Fe(OH)3发生还原反应 | ||
| C. | Cl2是氧化剂 | D. | 每生成1mol K2FeO4转移2mol电子 |
分析 2Fe(OH)3+3Cl2+10KOH $\frac{\underline{\;0~30℃\;}}{\;}$2K2FeO4+6KCl+8H2O反应中,Fe元素的化合价升高,被氧化,Cl元素的化合价降低,被还原,以此解答该题.
解答 解:2Fe(OH)3+3Cl2+10KOH $\frac{\underline{\;0~30℃\;}}{\;}$2K2FeO4+6KCl+8H2O反应中,Fe元素的化合价升高,被氧化,Cl元素的化合价降低,被还原,则Cl2是氧化剂,Fe(OH)3为还原剂,每生成1mol K2FeO4,消耗1.5mol氯气,转移3mol电子,只有C正确.
故选C.
点评 本题考查氧化还原反应,为高频考点,题目难度不大,注意从元素化合价的角度分析,注意氧化剂与还原剂的区别.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将Fe(OH)2露置在空气中加热灼烧可以得到FeO | |
| B. | 为防止FeSO4被氧化而变质,常在溶液中加入少量的铁粉 | |
| C. | 要证明某溶液中不含Fe3+而可能含Fe2+,先加氯水,再加少量的KSCN溶液 | |
| D. | 将浓硫酸与碳混合加热,生成的气体通入足量的澄清石灰水可检验气体产物中的CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3可以用于治疗胃酸过多 | |
| B. | 浓硝酸具有强氧化性,因此浓硝酸可以作为漂白剂 | |
| C. | SiO2可以用于生产太阳能电池 | |
| D. | 在FeCl3饱和溶液里通入足量NH3可制取Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为117,质子数为78的铂原子:${\;}_{117}^{195}$Pt | |
| B. | 氯离子的结构示意图: | |
| C. | 乙烯的结构简式:CH2CH2 | |
| D. | KCl的电子式: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
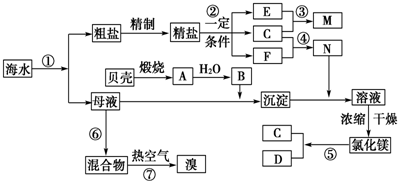 我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是某化工厂对海水资源综合利用的示意图:
我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是某化工厂对海水资源综合利用的示意图:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com