
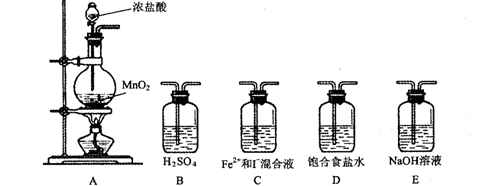
 (按氯气流向的顺序用序号书写)
(按氯气流向的顺序用序号书写) ⑵实验开始后,控制通入少量氯气,通过观察溶液颜色的变化, (能或不能)判断反应的先后顺序。
⑵实验开始后,控制通入少量氯气,通过观察溶液颜色的变化, (能或不能)判断反应的先后顺序。| 实验步骤 | 预期现象与结论 |
| 取少量反应的溶液置于A、B两支试管中; 向A试管中滴加 ; 向B试管中滴加 : | ① 若 则假设1成立 ② 若 则假设2成立 ③ 若 则假设3成立 |
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源:不详 题型:实验题
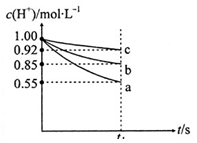
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
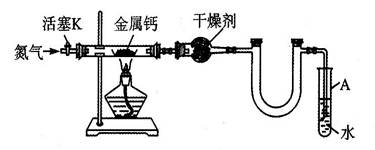
| 直玻管质量m0/g | 直玻管与钙的质量m1/g | 直玻管与产物的质量m2/g |
| 14.80 | 15.08 | 15.15 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
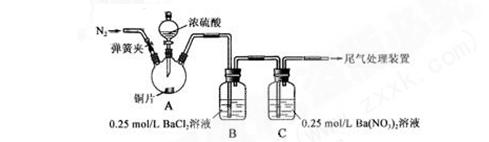
| 操作 | 现象 |
| 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C中产生白色沉淀,液面上放略显浅棕色并逐渐消失 |
| 打开弹簧夹,通入N2,停止加热,一段时间后关闭 | ___________________ |
| 从B、C中分别取少量白色沉淀,加稀盐酸 | 尚 未发现白色沉淀溶解 未发现白色沉淀溶解 |
 应。
应。 ①为证实各自的观点,在原实验基础上:甲在原有操作之前增加一步操作,该操作是_____________;
①为证实各自的观点,在原实验基础上:甲在原有操作之前增加一步操作,该操作是_____________;| 甲 | 大量白色沉淀 |
| 乙 | 少量白色沉淀 |
 于稀盐酸。结合离子方程式解释实验现象异同的原因:_____。
于稀盐酸。结合离子方程式解释实验现象异同的原因:_____。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
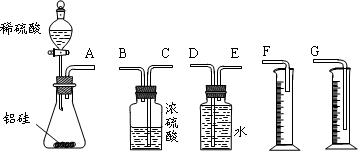
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
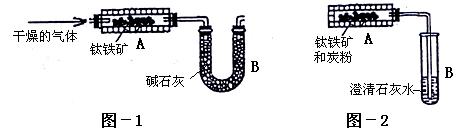
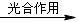 C6H12O6(葡萄糖)+6O2。
C6H12O6(葡萄糖)+6O2。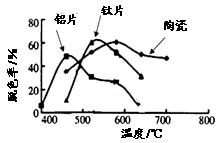
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| 实验 | 实验现象 | 结论 |
| A | 左边烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 | 活动性:Al>Fe>Cu |
| B | 烧瓶内颜色深浅不同 | 说明:2NO2 N2O4(g) △H<0 |
| C | 白色固体先变为淡黄色,后变为黑色 | 溶度积(Ksp):AgCl>AgBr >Ag2S |
| D | 锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
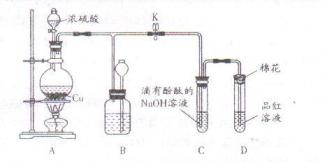
 直到反应完毕,最后发现烧瓶中还有铜片剩余。某同学根据所学的化学知识认为还有一定量的硫酸剩余。
直到反应完毕,最后发现烧瓶中还有铜片剩余。某同学根据所学的化学知识认为还有一定量的硫酸剩余。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com