
| A. | X元素在周期表中的位置只能是第二周期第ⅣA族 | |
| B. | 若X的常见简单阴离子Xn-能跟Y的单质发生氧化还原反应,则说明Y的非金属性比X的强 | |
| C. | 若Y的非金属性比X的强,则与同一种还原剂反应时,一个Y原子得到的电子数一定比一个X原子得到的电子数少 | |
| D. | 若X能形成XO32-、XO42-和X2O32-,Y能形成YO3-和XO4-,则X、Y一定在同一周期 |
分析 A.X、Y两种元素均为短周期元素,X元素的原子所具有的电子层数为其最外层电子数的二分之一,则X可能是He、C、S元素;
B.若X的常见简单阴离子Xn-能跟Y的单质发生氧化还原反应,则说明Y的非金属性比X的强;
C.非金属性强弱与得电子难易程度有关,与得电子多少无关;
D.若X能形成XO32-、XO42-和X2O32-,Y能形成YO3-和XO4-,则X是S元素、Y是Cl元素.
解答 解:A.元素在周期表中的位置可能是第二周期第ⅣA族,也可能是第三周期第ⅥA族,如为第3周期元素,则X为S,故A错误;
B.元素的非金属性越强,对应的单质的氧化性越强,若X的常见简单阴离子Xn-能跟Y的单质发生氧化还原反应置换出X,则说明Y的非金属性比X的强,故B正确;
C.元素的非金属性与得电子难易有关,与得电子多少无关,如二者不在同一周期,则一个Y原子得到的电子数不一定比一个X原子得到的电子数少,如:N原子得电子比S原子多,O原子与S原子同,故C错误;
D.若X能形成XO32-、XO42-和X2O32-,则X为S元素,Y能形成YO3-和YO4-,Y为Cl元素,二者在同一周期,故D正确.
故选:BD.
点评 本题考查位置结构性质的相互关系应用,题目难度中等,侧重考查原子的核外电子排布特点,同时考查学生发散思维能力,熟练掌握原子结构、元素周期表结构.


 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源: 题型:解答题
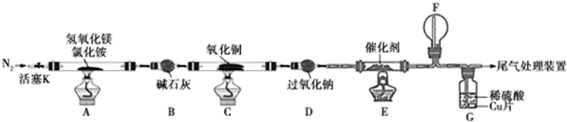
| 实验步骤 | 预期现象和结论 |
| 步骤1:取装置C中反应后的少许固体于试管中 | \ |
| 步骤2:向试管中加入2mol/LH2SO4溶液 | 液中出现蓝色,说明红色固体中含有Cu2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
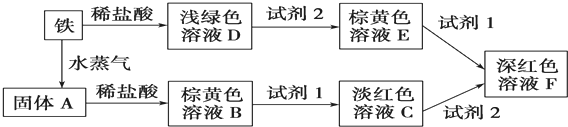
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2X2+3Y2?2X2Y3 | B. | 3X2+2Y2?2X3Y2 | C. | X2+2Y2?XY2 | D. | 2X2+Y2?2X2Y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硝酸是一种重要的工业原料,工业制硝酸的关键是氨的催化氧化,与硝酸工业相关的过程中产生的氮氧化物的处理与应用也是科学研究的热点.
硝酸是一种重要的工业原料,工业制硝酸的关键是氨的催化氧化,与硝酸工业相关的过程中产生的氮氧化物的处理与应用也是科学研究的热点.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Mg(HCO3)2溶液中加入过量的NaOH溶液Mg2++2HCO3-+2OH-═MgCO3↓+CO32-+2H2O | |
| B. | 溴化亚铁溶液中通入足量的氯气:2Fe2++Cl2═2Fe3++2Cl- | |
| C. | 少量的CO2通入稀的碳酸钠溶液中:CO2+CO32-+H2O═2HCO3- | |
| D. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2使SO42-反应完全2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com