
下列离子方程式正确的是( )
A. Cl2通入水中:Cl2+H2O═2H++Cl﹣+ClO﹣
B. 双氧水中加入稀硫酸和KI溶液:H2O2+2H++2I﹣═I2+2H2O
C. 用铜作电极电解CuSO4溶液:2Cu2++2H2O 2Cu+O2↑+4H+
2Cu+O2↑+4H+
D. Na2S2O3溶液中加入稀硫酸:2S2O32﹣+4H+═SO42﹣+3S↓+2H2O
考点: 离子方程式的书写.
专题: 离子反应专题.
分析: A.HClO为弱酸,在离子反应中保留化学式;
B.发生氧化还原反应生成硫酸钾、碘、水;
C.铜作电解,阳极Cu失去电子,实质为电镀;
D.发生氧化还原反应生成S、SO2、H2O.
解答: 解:A.Cl2通入水中的离子反应为Cl2+H2O⇌H++Cl﹣+HClO,故A错误;
B.双氧水中加入稀硫酸和KI溶液的离子反应为H2O2+2H++2I﹣═I2+2H2O,故B正确;
C.用铜作电极电解CuSO4溶液,实质为电镀,阳极Cu失去电子,阴极铜离子得电子,故C错误;
D.Na2S2O3溶液中加入稀硫酸的离子反应为S2O32﹣+2H+═SO2↑+S↓+H2O,故D错误;
故选B.
点评: 本题考查离子反应的书写,明确发生的化学反应是解答本题的关键,注意发生的氧化还原反应为解答的难点,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
(NH4)2SO4在一定条件下发生如下反应:4(NH4)2SO4=N2↑+6NH3↑+3SO2↑+SO3↑+7H2O,将反应后的混合气体通入BaCl2溶液,产生的沉淀为()
A. BaSO4 B. BaSO3 C. BaS D. BaSO4和BaSO3
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:①2K2CrO4+H2SO4=K2Cr2O7+K2SO4+H2O;②Fe2(SO4)3+2HI=2FeSO4+I2+H2SO4;
③K2Cr2O7+FeSO4+H2SO4═Fe2(SO4)3+Cr2(SO4)3+K2SO4+H2O
(1)上述三个反应中,属于氧化还原反应的是 (填序号);
(2)配平反应③的化学方程式并用双线桥表示电子转移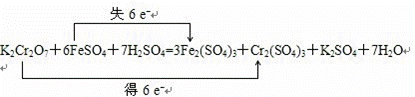 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
NA为阿伏伽德罗常数的值,下列叙述正确的是( )
A. 1.0L 1.0mo1•L﹣1的NaAlO2水溶液中含有的氧原子数为2NA
B. 12g石墨烯(单层石墨)中含有六元环的个数为0.5NA
C. 25℃时pH=13的NaOH溶液中含有OH﹣的数目为0.1NA
D. 1mol的羟基与1moL的氢氧根离子所含电子数均为9NA
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,下列微粒的还原性顺序为Cl﹣<Br﹣<Fe2+<I﹣<SO2,由此判断以下各反应在溶液中不能发生的是( )
A. 2Fe3++SO2+2H2O═2Fe2++SO42﹣+4H+
B. 2Fe2++Cl2═2Fe3++2Cl﹣
C. 2Br﹣+4H++SO42﹣═SO2+Br2+2H2O
D. I2+SO2+2H2O═4H++SO42﹣+2I﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
有一含NaCl、Na2CO3•10H2O和NaHCO3的混合物,某同学设计如下实验,通过测量反应前后C、D装置质量的变化,测定该混合物中各组分的质量分数.
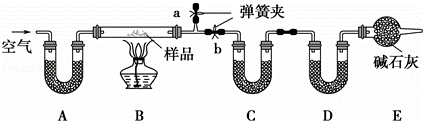
(1)加热前通入空气的目的是 ,操作方法为 .
装置A、C、D中盛放的试剂分别为:A ,C ,D .
(3)若将A装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl的含量将 (填“偏高”、“偏低”或“无影响”,下同);若B中反应管右侧有水蒸气冷凝,则测定结果中NaHCO3的含量将 ;若撤去E装置,则测得Na2CO3•10H2O的含量将 .
(4)若样品质量为wg,反应后C、D增加的质量分别为m1g、m2g,由此可知混合物中NaHCO3的质量分数为 % (用含w、m1、m2的代数式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法正确的是()
A. 信息产业中的光缆的主要成份是单质硅
B. 利用激光笔可以区别鸡蛋清和浓盐水
C. 油脂、糖类、蛋白质都属于天然高分子化合物
D. 煤经气化、液化和干馏三个物理变化过程,可变为清洁能源
查看答案和解析>>
科目:高中化学 来源: 题型:
2001年9月1日将执行国家食品卫生标准规定,酱油中3﹣氯丙醇(ClCH2CH2CH2OH)含量不得超过1ppm.相对分子质量为94.5的氯丙醇(不含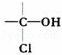 结构)共有( )
结构)共有( )
A. 5种 B. 4种 C. 3种 D. 2种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com