
【题目】请回答下列问题:
Ⅰ.一定条件下,A(g)+B(g) ![]() C(g) ΔH<0,达到平衡后根据下列图象判断:
C(g) ΔH<0,达到平衡后根据下列图象判断:
A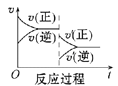 B
B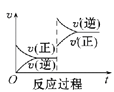 C
C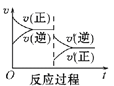 D
D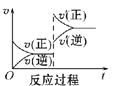
(1)升高温度,达到新平衡的是_____(选填字母),新平衡中C的体积分数______(选填“增大”“减小”或“不变”)。
(2)减小压强,达到新平衡的是________(选填字母),A的转化率________(选填“增大”“减小”或“不变”)。
Ⅱ. 取五等份NO2,分别充入五个温度不同、容积相同的恒容密闭容器中,发生反应:2NO2(g) ![]() N2O4(g) ΔH<0,反应一段时间后,分别测定体系中NO2的体积分数,并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是___。
N2O4(g) ΔH<0,反应一段时间后,分别测定体系中NO2的体积分数,并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是___。
①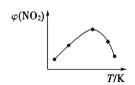 ②
②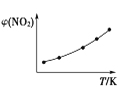 ③
③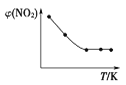 ④
④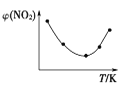
【答案】B 减小 C 减小 ②④
【解析】
Ⅰ.(1)该反应为放热反应,升高温度,反应速率加快,平衡逆向移动;
(2)减小压强,平衡向着体积增大的方向移动,即平衡逆向移动;
Ⅱ. 在恒容的状态下,在五个相同容积的容器中通入等量的NO2,达到平衡状态之前,温度越高,反应速率越快,达到平衡状态后,温度升高,平衡逆向移动;
Ⅰ.(1)该反应为放热反应,升高温度,反应速率加快,v(正)、v(逆)整体增大,平衡逆向移动,v(逆)>v(正),因此升高温度,达到新平衡的图是B;平衡逆向移动,平衡中C的体积分数减小;
(2)减小压强,平衡逆向移动,v(正)、v(逆)整体减小,且v(逆)>v(正),为图C;平衡逆向移动,A的转化率减小;
Ⅱ. 达到平衡状态之前,温度越高,反应速率越快,NO2的体积分数越来越小,达到平衡状态后,温度升高,平衡逆向移动,NO2的体积分数逐渐增大,因此可能与实验结果相符的图为②④;


科目:高中化学 来源: 题型:
【题目】下列关于水的污染和污水处理的知识错误的是( )
A.赤潮不属于植物营养物质污染
B.震惊世界的日本水蜈病和疼痛病是由重金属污染引起的
C.处理含有重金属离子的污水可用沉淀法
D.混凝法中明矾处理污水的化学原理可表示为Al3++3H2O![]() Al(OH)3(胶体)+3H+
Al(OH)3(胶体)+3H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离平衡常数如下表:
弱酸 | HCOOH | HCN | H2CO3 |
电离平衡常数(25℃) | Ka=1.77×10-4 | Ka=5.0×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
①HCOONa、NaCN、NaHCO3、Na2CO3这四种溶液的阴离子结合质子能力最强的是______。
②体积相同、c(H+)相同的三种酸溶液a.HCOOH;b.HCN;c.H2SO4分别与浓度相等的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的排列顺序是(填序号)_____。
③向NaCN溶液通入少量CO2反应的化学方程式是_______。
(2)一定浓度的NaCN溶液pH=9,用离子方程式表示呈碱性的原因是____,此时, =_____。
=_____。
(3)常温下,向20 mL 0.1 mol/L Na2CO3溶液中逐滴加入0.1 mol/L HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。
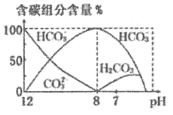
回答下列问题:
在同一溶液中H2CO3、![]() 、
、![]() ______(填“能”或“不能”)大量共存。
______(填“能”或“不能”)大量共存。
②当pH=7时,溶液中含碳元素的主要微粒为_____,溶液中各种离子(![]() 除外)的物质的量浓度的大小关系为______。
除外)的物质的量浓度的大小关系为______。
③已知在25℃时,![]() 水解反应的平衡常数即水解常数Kh=
水解反应的平衡常数即水解常数Kh=![]() =2.0×10-4,当溶液中c(
=2.0×10-4,当溶液中c(![]() ):c(
):c(![]() )=2:1时,溶液pH=______。
)=2:1时,溶液pH=______。
(4)已知CaCO3的Ksp=2.8×10-9,现将浓度为2×10-4 mol/L Na2CO3溶液与CaCl2溶液等体积混合,则生成CaCO3沉淀所需CaCl2溶液的最小浓度为________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是芳香族化合物,其分子式为C9H11Cl,利用A合成2-甲基苯乙酸,其合成路线如下:

(1)A结构简式为_____________。
(2)A→B反应类型为_______;C中所含官能团的名称为______________。
(3)C→D第①步的化学方程式为____________。
(4)在NaOH醇溶液并加热的条件下,A转化为E,符合下列条件的E的同分异构体有___种,任写其中一种的结构简式____________。
i,苯环上仅有一个取代基;ii.能与溴水发生加成反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】改变0.1![]() 二元弱酸
二元弱酸![]() 溶液的pH,溶液中的
溶液的pH,溶液中的![]() 、
、![]() 、
、![]() 的物质的量分数
的物质的量分数![]() 随pH的变化如图所示[已知
随pH的变化如图所示[已知 ]。
]。

下列叙述错误的是( )
A. pH=1.2时, ![]()
B. ![]()
C. pH=2.7时, ![]()
D. pH=4.2时, ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请完成下列物质的分离提纯问题。
Ⅰ.现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去溶液中的NaCl和Na2SO4,从而得到纯净的NaNO3溶液。相应的实验过程可用下图表示:

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X_______。
(2)证明AgNO3溶液加过量的实验方是_____________________________________________ 。(3)按此实验方案得到的溶液3中肯定含有__________(填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的___________(填化学式),之后若要获得固体NaNO3需进行的实验操作是___________(填操作名称)。
Ⅱ.某同学欲用CCl4萃取较高浓度的碘水中的碘,操作过程可以分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50ml碘水和15mlCCl4加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层液体;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;
H.静置、分层。
(1)萃取过程正确操作步骤的顺序是:_________________________________ (填编号字母)。
(2)从含碘的CCl4溶液中提取碘 和回收CCl4,还需要经过蒸馏,观察下图所示实验装置指出其错误有______ 处。
(3)进行上述蒸馏操作时,最后晶态碘在____________(填仪器名称)里聚集。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中可提取多种化工原料,下面是工业上对海水成分综合利用的示意图。
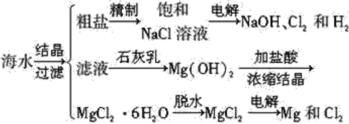
试回答下列问题:
(1)写出用海滩上的贝壳制Ca(OH)2的化学方程式_________________________。
(2)写出电解饱和NaCl溶液的化学方程式___________________________________。
(3)将电解生成的氯气通入石灰乳中可制得漂白粉,写出其反应的化学方程式_______________________。
(4)用海滩上的贝壳制Ca(OH)2而不从异地山中开凿石灰石制取,主要考虑到什么问题?_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X的蒸气相对氢气的密度为51,X中氧元素的质量分数为31.5%,则能与NaOH溶液发生反应的X的同分异构体有(不考虑立体异构)( )
A. 15种B. 14种C. 13种D. 12种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CMU是一种荧光指示剂,可通过下列反应制备:
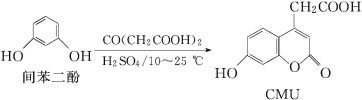
下列说法正确的是( )
A.1 mol CMU最多可与4 mol Br2反应
B.1 mol CMU最多可与4 mol NaOH反应
C.可用FeCl3溶液鉴别间苯二酚和CMU
D.CMU在酸性条件下的水解产物只有1种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com