
【题目】能正确表示下列反应的离子方程式是( )
A. 用过量氨水吸收工业尾气中的SO2:2NH3H2O+SO2=2NH4++SO32-+H2O
B. 氯化钠与浓硫酸混合加热:H2SO4+2Cl-![]() SO2↑+Cl2↑+H2O
SO2↑+Cl2↑+H2O
C. 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O
D. 明矾溶液中滴入Ba(OH)2溶液使SO42-,恰好完全沉淀:2Ba2++3OH-+Al3++2SO42-═2BaSO4↓+Al(OH)3↓
【答案】A
【解析】
A.用过量氨水吸收工业尾气中的SO2的离子反应为2NH3H2O+SO2═2NH4++SO32-+H2O,故A正确;
B.氯化钠与浓硫酸混合加热,浓硫酸中只有很少的水,氯化钠几乎不能电离,故该反应的离子方程式就是其化学方程式,H2SO4+2NaCl ![]() Na2SO4+2HCl↑,故B错误;
Na2SO4+2HCl↑,故B错误;
C.磁性氧化铁的主要成分为四氧化三铁,溶于稀硝酸的离子反应方程式为3Fe3O4+28H++NO3-═9Fe3++NO↑+14H2O,故C错误;
D.明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀的离子反应方程式为2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O,故D错误;
答案选A。


科目:高中化学 来源: 题型:
【题目】298 K时,AgSCN的沉淀溶解平衡曲线如图所示,下列判断错误的是

A. 298 K时,Ksp(AgSCN)=1.0×10-12
B. 欲使溶液由c点移到d点,可滴入少量KSCN浓溶液
C. 向a点溶液中加入等物质的量的AgNO3、KSCN固体后,可能使a点移动到c点
D. b点溶液蒸发部分水后恢复至室温可移动到c点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组以化合物1为原料,按下列路线制备聚合物8。

已知:R—X![]() R—CN
R—CN![]() R—COOH
R—COOH
R—CH2COOH![]()
![]()
请回答:
(1)以下四个化合物中,含有羧基的是
A.化合物3 B.化合物4 C.化合物6 D.化合物7
(2)化合物4→8的合成路线中,未涉及的反应类型是
A.取代反应 B.消去反应 C.加聚反应 D.还原反应
(3)下列四个化合物中,与化合物4互为同系物的是
A.CH3COOC2H5B.C6H5COOH
C.CH3CH2CH2COOH D.CH3COOH
(4)化合物4的属于酯类的所有同分异构体的结构简式 。
(5)化合物7→8的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置进行实验,下列对实验现象的解释不合理的是

选项 | ①试剂 | ①中现象 | 解释 |
A | 品红溶液 | 溶液褪色 | SO2具有漂白性 |
B | Na2SiO3溶液 | 产生胶状沉淀 | 酸性: H2SO3 >H2SiO3 |
C | 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |
D | Ba(NO3)2溶液 | 生成白色沉淀 | SO32-与Ba2+生成 白色BaSO3沉淀 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某浓差电池的原理示意如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。下列有关该电池的说法正确的是

A. 电子由X极通过外电路移向Y极
B. 电池工作时,Li+通过离子导体移向b区
C. 负极发生的反应为:2H++2e-=H2↑
D. Y极每生成1 mol Cl2,a区得到2 mol LiCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是以秸秆(含多糖类物质)为原料合成聚酯类高分子化合物的路线:

已知:
请回答下列问题:
食物中的纤维素虽然不能为人体直接提供能量,但能促进肠道蠕动,黏附并带出有害物质,俗称人体内的“清道夫”。从纤维素的化学成分看,它是一种____(填序号)。
a.单糖 b.多糖 c.氨基酸 d.脂肪
A中官能团的名称为____、____。
A生成B的反应条件为____。
B、C的结构简式分别为____、____。
写出E→F的化学反应方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】门捷列夫在研究周期表时预言了包括“类铝”、“类硅”在内的11种元素。
(1)门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现,命名为锗(Ge)。
①已知主族元素锗的最高化合价为+4价,其最高价氧化物的水化物为两性氢氧化物。试比较元素的非金属性Si___ Ge(用“>”或“<”表示)。
②若锗位于Si的下一周期,写出“锗”在周期表中的位置_____。根据锗在周期表中处于金属和非金属分界线附近,预测锗单质的一种用途是_______.
③硅和锗单质分别与![]() 反应时,反应较难进行的是_______(填“硅”或“锗”)。
反应时,反应较难进行的是_______(填“硅”或“锗”)。
(2)“类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。
①由镓的性质推知,镓与铝同主族,且位于铝的下一周期。试写出镓原子的结构示意图____。冶炼金属镓通常采用的方法是_____.
②已知Ga(OH)3难溶于水,为判断Ga(OH)3是否为两性氢氧化物,设计实验时,需要选用的试剂有GaCl3溶液、________和________.
(3)某同学阅读课外资料,看到了下列有关锗、锡、铅三种元素的性质描述:
①锗、锡在空气中不反应,铅在空气中表面形成一层氧化铅;
②锗与盐酸不反应,锡与盐酸反应,铅与盐酸反应但生成PbCl2微溶而使反应终止:
该同学查找三种元素在周期表的位置如图所示:
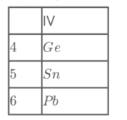
根据以上信息推测,下列描述正确的是______(填标号)。
a.锗、锡、铅的+4价的氢氧化物的碱性强弱顺序是:Ge(OH)4<Sn(OH)4<Pb(OH)4
b.锗、锡、铅的金属性依次减弱;
c. 锗、锡、铅的原子半径依次增大。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E五种元素,它们的质子数依次增多。
①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体;
②A和B两元素可形成B2A3化合物,该化合物既能溶于强酸,又能溶于强碱;
③C+离子比B3+离子多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥E、C同主族,且E比C多两个电子层,E单质可与冷水反应生成氢气。
试回答:
(1)写出元素C、E的名称:C______;E______。
(2)画出A的原子结构示意图______,B的离子结构示意图______,D的单质分子的电子式______。
(3)写出B2A3分别与盐酸和氢氧化钠溶液反应的离子方程式:
____________________;___________________。
(4)比较B、C、E三种元素形成的简单离子半径的大小和氧化性的强弱(用离子符号表示):离子半径:_____________;氧化性:____________。
(5)写出E与冷水反应的化学方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物A~H的转换关系如下所示:

请回答下列问题:
(1)链烃A有支链且只有一个官能团,其相对分子质量在65~75之间,1 mol A完全燃烧消耗7 mol氧气,则A的结构简式是____________________________。
(2)在特定催化剂作用下,A与等物质的量的H2反应生成E。E______(填“存在”或“不存在”)顺反异构,由E转化为F的化学方程式为______________________________。
(3)G与金属钠反应能放出气体,由F转化为G的反应条件是__________________;由G生成H的化学方程式是__________________。
(4)B是A的一种同分异构体,它的一氯代物只有一种(不考虑立体异构),则B的结构简式为________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com