
| A | B | C | D | |
| Ą¬»ų·ÖĄą | ·ĻŅץ¹Ž | ²»æÉŌŁÉś·ĻÖ½ | ·Ļµē³Ų | ·ĻĖÜĮĻĘæ |
 æÉ»ŲŹÕĪļ |  æÉČ¼Ą¬»ų |  ÓŠŗ¦Ą¬»ų |  ĘäĖüĄ¬»ų |
| A£® | A | B£® | B | C£® | C | D£® | D |
·ÖĪö A£®·ĻŅץ¹ŽÖ÷ŅŖ²ÄĮĻĪŖĀĮÖŹ£¬ĀĮæÉ»ŲŹÕ£»
B£®·ĻÖ½ŗ¬ÓŠ“óĮæĻĖĪ¬£¬æÉŅŌČ¼ÉÕ£»
C£®·Ļµē³ŲÖŠŗ¬ÓŠÖŲ½šŹōµČÓŠŗ¦ĪļÖŹ£»
D£®·ĻĖÜĮĻĘæÖ÷ŅŖÓɾŪŅŅĻ©»ņ¾Ū±ūĻ©ÖĘŌģ¶ų³É£¬æÉ»ŲŹÕĄūÓĆ£®
½ā“š ½ā£ŗA£®·ĻŅץ¹ŽÖ÷ŅŖ²ÄĮĻĪŖĀĮÖŹ£¬ŹōÓŚæÉ»ŲŹÕĄūÓĆµÄ²ÄĮĻ£¬ŹōÓŚæÉ»ŲŹÕĪļ£¬¹ŹAÕżČ·£»
B£®·ĻÖ½ŗ¬ÓŠ“óĮæĻĖĪ¬£¬æÉŅŌČ¼ÉÕ£¬ĖłŅŌŹōÓŚæÉČ¼Ą¬»ų£¬¹ŹBÕżČ·£»
C£®·Ļµē³ŲÖŠŗ¬ÓŠÖŲ½šŹōµČÓŠŗ¦ĪļÖŹ£¬ĖłŅŌŹōÓŚÓŠŗ¦Ą¬»ų£¬¹ŹCÕżČ·£»
D£®·ĻĖÜĮĻĘæÖ÷ŅŖÓɾŪŅŅĻ©»ņ¾Ū±ūĻ©ÖĘŌģ¶ų³É£¬Ņ²æÉ»ŲŹÕĄūÓĆ£¬ĖłŅŌŹōÓŚæÉ»ŲŹÕĪļ£¬¹ŹD“ķĪó£®
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²é»ÆѧŹŌ¼ĮµÄ·ÖĄą£¬ÄŃ¶Č²»“ó£¬æÉ»ŲŹÕĄ¬»ųÖ÷ŅŖ°üĄØ·ĻÖ½”¢ĖÜĮĻ”¢²£Į§”¢½šŹōŗĶ²¼ĮĻĪå“óĄą£¬Ķعż×ŪŗĻ“¦Ąķ»ŲŹÕĄūÓĆ£¬æÉŅŌ¼õÉŁĪŪČ¾£¬½ŚŹ”׏Ō“£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
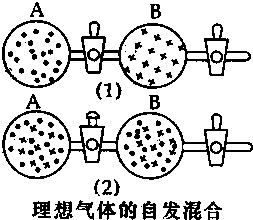 ŌŚĶ¼£Ø1£©ÖŠA”¢BĮ½øöČŻĘ÷Ąļ£¬·Ö±šŹÕ¼Æ×ÅĮ½øö×÷ÓĆ²»Ķ¬µÄĄķĻėĘųĢ壮Čō½«ÖŠ¼ä»īČū“ņæŖ[ČēĶ¼£Ø2£©]£¬Į½ÖÖĘųĢå·Ö×ÓĮ¢¼“¶¼Õ¼ÓŠĮĖĮ½øöČŻĘ÷£®ÕāŹĒŅ»øö²»°éĖęÄÜĮæ±ä»ÆµÄ×Ō·¢¹ż³Ģ£®¹ŲÓŚ“Ė¹ż³ĢµÄĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
ŌŚĶ¼£Ø1£©ÖŠA”¢BĮ½øöČŻĘ÷Ąļ£¬·Ö±šŹÕ¼Æ×ÅĮ½øö×÷ÓĆ²»Ķ¬µÄĄķĻėĘųĢ壮Čō½«ÖŠ¼ä»īČū“ņæŖ[ČēĶ¼£Ø2£©]£¬Į½ÖÖĘųĢå·Ö×ÓĮ¢¼“¶¼Õ¼ÓŠĮĖĮ½øöČŻĘ÷£®ÕāŹĒŅ»øö²»°éĖęÄÜĮæ±ä»ÆµÄ×Ō·¢¹ż³Ģ£®¹ŲÓŚ“Ė¹ż³ĢµÄĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | “Ė¹ż³ĢŹĒ“Ó»ģĀŅ³Ģ¶ČŠ”µÄĻņ»ģĀŅ³Ģ¶Č“ó±ä»Æ¹ż³Ģ£¬¼“ģŲŌö“óµÄ¹ż³Ģ | |
| B£® | “Ė¹ż³ĢĪŖ×Ō·¢¹ż³Ģ£¬¶ųĒŅƻӊČČĮæµÄĪüŹÕ»ņ·Å³ö | |
| C£® | “Ė¹ż³Ģ“ÓÓŠŠņµ½ĪŽŠņ£¬»ģĀŅ¶ČŌö“ó | |
| D£® | “Ė¹ż³ĢŹĒ×Ō·¢æÉÄęµÄ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ¢ŚŗĶ¢Ū¾łŹōÓŚĻ©ĢžĄą | B£® | ¢ŁŗĶ¢Ū»„ĪŖĶ¬·ÖŅģ¹¹Ģå | ||
| C£® | ¢ÜŹĒ¢ŚµÄŃõ»Æ²śĪļ | D£® | ¢ŪŗĶ¢Ü¾łÄÜ·¢ÉśĻūČ„”¢õ„»Æ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

| ĪļÖŹ | ¼× | ŅŅ | ±ū |  |
| Ī¢¹ŪŹ¾ŅāĶ¼ |  |  | 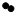 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | »·ŅŃĶéµÄ½į¹¹¼ņŹ½ 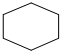 | B£® | C2H4µÄĒņ¹÷Ä£ŠĶ | ||
| C£® | ĖÄĀČ»ÆĢ¼µÄµē×ÓŹ½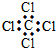 | D£® | ±½µÄ·Ö×ÓŹ½ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ö»ÓŠ¢Ś¢Ü¢Ž | B£® | Ö»ÓŠ¢Ł¢Ż¢Ž | C£® | Ö»ÓŠ¢Ł¢Ś¢Ū¢Ż¢Ž | D£® | Č«²æ¶¼æÉŅŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼×ĶéµÄ±ź×¼Č¼ÉÕČČĪŖ-890.3kJ•mol-1£¬Ōņ¼×ĶéČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖ£ŗCH4£Øg£©+2O2£Øg£©ØTCO2£Øg£©+2H2O£Øl£©”÷H=-890.3kJ•mol-1 | |
| B£® | 500”ę”¢30MPaĻĀ£¬½«0.5mol N2ŗĶ1.5molH2ÖĆÓŚĆܱյÄČŻĘ÷ÖŠ³ä·Ö·“Ӧɜ³ÉNH3£Øg£©£¬·ÅČČ19.3kJ£¬ĘäČČ»Æѧ·½³ĢŹ½ĪŖ£ŗN2£Øg£©+3H2£Øg£©$\frac{\underline{\;\;\;\;\;“߻ƼĮ\;\;\;\;\;}}{500”ę30MPa}$ 2NH3£Øg£©”÷H=-38.6kJ•mol-1 | |
| C£® | ĀČ»ÆĆ¾ČÜŅŗÓė°±Ė®·“Ó¦£ŗMg2++2OH-ØTMg£ØOH£©2”ż | |
| D£® | Ńõ»ÆĀĮČÜÓŚNaOHČÜŅŗ£ŗAl2O3+2OH-+3H2OØT2Al£ØOH£©3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
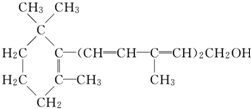
| A£® | Ī¬ÉśĖŲAŹĒŅ»ÖÖ“¼ | |
| B£® | Ī¬ÉśĖŲAµÄŅ»øö·Ö×ÓÖŠŗ¬ÓŠČżøöĢ¼Ģ¼Ė«¼ü | |
| C£® | Ī¬ÉśĖŲAµÄŅ»øö·Ö×ÓÖŠÓŠ33øöĒāŌ×Ó | |
| D£® | Ī¬ÉśĖŲA²»ÄÜŹ¹äåµÄCCl4ČÜŅŗĶŹÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŌŖĖŲ | Ļą¹ŲŠÅĻ¢ |
| T | TŌ×ÓĖł“¦µÄÖÜĘŚŹż”¢×åŠņŹż·Ö±šÓėĘäŌ×ÓŠņŹżĻąµČ |
| X | XµÄ»łĢ¬Ō×ÓÖŠµē×ÓÕ¼¾ŻČżÖÖÄÜĮæ²»Ķ¬µÄŌ×Ó¹ģµĄ£¬ĒŅĆæÖÖ¹ģµĄÖŠµÄµē×ÓŹżĻąĶ¬ |
| Z | ZµÄ»łĢ¬Ō×Ó¼Ūµē×ÓÅŲ¼ĪŖns2npn+2 |
| Q | ŌŚøĆŌŖĖŲĖłŌŚÖÜĘŚÖŠ£¬QµÄ»łĢ¬Ō×ӵĵŚŅ»µēĄėÄÜ×īŠ” |
| R | 3pÄܼ¶ÉĻÓŠ1øöµē×Ó |
| W | WµÄŅ»ÖÖŗĖĖŲµÄÖŹĮæŹżĪŖ65£¬ÖŠ×ÓŹżĪŖ36 |
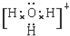 £®CĪŖ4øöŌ×ÓŗĖ¹¹³ÉµÄ·Ö×Ó£¬ŌņÓėC»„ĪŖµČµē×ÓĢåµÄ·Ö×ÓæÉŅŌŹĒ
£®CĪŖ4øöŌ×ÓŗĖ¹¹³ÉµÄ·Ö×Ó£¬ŌņÓėC»„ĪŖµČµē×ÓĢåµÄ·Ö×ÓæÉŅŌŹĒ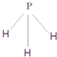 £ØŠ“½į¹¹Ź½£©£®D·Ö×ÓÖŠĮ½ŌŖĖŲµÄŌ×ÓøöŹżÖ®±ČĪŖ1£ŗ1£¬ŌņDĪŖ¼«ŠŌ£ØĢī”°¼«ŠŌ”±»ņ”°·Ē¼«ŠŌ”±£©·Ö×Ó£®Ä³Ė«Ō×Óµ„ÖŹ·Ö×ÓEŅ²ĪŖ18µē×ÓĪ¢Į££¬EÓėĖ®µÄ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ2F2+2H2O=4HF+O2£®
£ØŠ“½į¹¹Ź½£©£®D·Ö×ÓÖŠĮ½ŌŖĖŲµÄŌ×ÓøöŹżÖ®±ČĪŖ1£ŗ1£¬ŌņDĪŖ¼«ŠŌ£ØĢī”°¼«ŠŌ”±»ņ”°·Ē¼«ŠŌ”±£©·Ö×Ó£®Ä³Ė«Ō×Óµ„ÖŹ·Ö×ÓEŅ²ĪŖ18µē×ÓĪ¢Į££¬EÓėĖ®µÄ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ2F2+2H2O=4HF+O2£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com