
(1)有关Na2O2起反应的化学方程式是______________________________________。
(2)CH4、O2、Na2O2的物质的量之比是______________________________________。
(3)取0.1 mol CH4,向残余固体加足量的酸,能放出________mol气体。
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
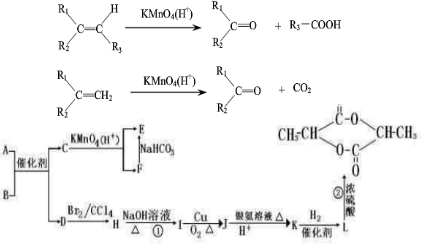


| 一定条件 |
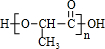 +(n-1)H2O
+(n-1)H2O| 一定条件 |
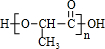 +(n-1)H2O
+(n-1)H2O

查看答案和解析>>
科目:高中化学 来源: 题型:
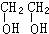
查看答案和解析>>
科目:高中化学 来源:黄冈重点作业·高二化学(下) 题型:021
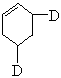
已知1,3-丁二烯CH2=CH-CH=CH2的C=C与C-C相间隔(化学上属共轭二烯烃)是非常重要的二烯烃,当其与等物质的量的Br2加成时有两种生成物:1,2-加成产物为CH2Br-CHBr-CH=CH2;1,4-加成产物为CH2Br-CH=CH-CH2Br.将结构简式为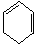 的烃跟D2(重氢)以等物质的量混合,并在一定条件下反应,所得产物的结构简式可能是
的烃跟D2(重氢)以等物质的量混合,并在一定条件下反应,所得产物的结构简式可能是
[ ]



查看答案和解析>>
科目:高中化学 来源:2013-2014学年山西省四校高三第四次联考理综化学试卷(解析版) 题型:填空题
甲醇燃料分为甲醇汽油和甲醇柴油。工业上合成甲醇的方法很多。
(1)一定条件下发生反应:
①CO2(g) +3H2(g) =CH3OH(g)+H2O(g) ? △H1????
②2CO(g) +O2(g) =2CO2(g)?? △H2
③2H2(g)+O2(g) =2H2O(g)????????? △H3
则CO(g) + 2H2(g)  CH3OH(g) 的△H=??????????????? 。
CH3OH(g) 的△H=??????????????? 。
(2)在容积为2L的密闭容器中进行反应: CO(g)+2H2(g) CH3OH(g) ,其他条件不变,在300℃和500℃时,物质的量n(CH3OH) 与反应时间t的变化曲线如图所示。该反应的△H???? 0 (填>、<或=)。
CH3OH(g) ,其他条件不变,在300℃和500℃时,物质的量n(CH3OH) 与反应时间t的变化曲线如图所示。该反应的△H???? 0 (填>、<或=)。
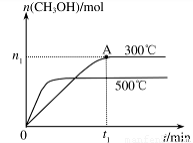
(3)若要提高甲醇的产率,可采取的措施有____________(填字母)。
A.缩小容器体积
B.降低温度
C.升高温度
D.使用合适的催化剂
E.将甲醇从混合体系中分离出来
(4)CH4和H2O在催化剂表面发生反应CH4+H2O CO+3H2,T℃时,向1 L密闭容器中投入1 mol CH4和1 mol H2O(g),5小时后测得反应体系达到平衡状态,此时CH4的转化率为50% ,计算该温度下的平衡常数???? (结果保留小数点后两位数字)。
CO+3H2,T℃时,向1 L密闭容器中投入1 mol CH4和1 mol H2O(g),5小时后测得反应体系达到平衡状态,此时CH4的转化率为50% ,计算该温度下的平衡常数???? (结果保留小数点后两位数字)。
(5)以甲醇为燃料的新型电池,其成本大大低于以氢为燃料的传统燃料电池,目前得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:
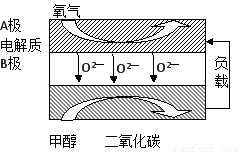
①B极的电极反应式为????????????????????? 。
②若用该燃料电池做电源,用石墨做电极电解硫酸铜溶液,当电路中转移1mole- 时,实际上消耗的甲醇的质量比理论上大,可能原因是????????????????????? 。
(6)25℃时,草酸钙的Ksp=4.0×10-8,碳酸钙的Ksp=2.5×10-9。向20ml碳酸钙的饱和溶液中逐滴加入8.0×10-4 mol·L-1的草酸钾溶液20ml,能否产生沉淀?????? (填“能”或“否”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com