

| 物质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| 沸点/℃ | 57.7 | 12.8 | - | 315 | - |
| 熔点/℃ | -70.0 | -107.2 | - | - | - |
| 升华温度/℃ | - | - | 180 | 300 | 162 |
| ||
| ||


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
| A、在一定条件下,催化分解80g SO3,混合气体中含有的氧原子数为3NA |
| B、一定条件下,铁与水蒸气反应生成8.96L(已折合成标准状况)H2时,转移的电子数为0.8NA |
| C、各取1mol/L AlCl3与3mol/L NaCl溶液100mL混合后,溶液中所含Cl-数为0.6NA |
| D、含有非极性键的数目为NA的Na2O2与水充分反应,标准状况下产生22.4L O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.现用该浓硫酸配制100mL 1mol/L的稀硫酸.可供选用的仪器有:
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.现用该浓硫酸配制100mL 1mol/L的稀硫酸.可供选用的仪器有:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
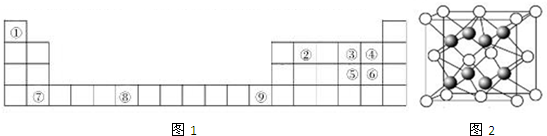
查看答案和解析>>
科目:高中化学 来源: 题型:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、甲醛的电子式: |
B、 的名称:3-甲基-2-丁烯 的名称:3-甲基-2-丁烯 |
C、原子结构示意图: 表示12C,也可以表示13C 表示12C,也可以表示13C |
| D、纯碱溶液呈碱性的原因:C032-+2H20═H2C03+20H- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com