
| 容器 | 甲 | 乙 |
| 反应物投入量 | 3molFe、2molCO2 | 4molFeO、3molCO |
| CO的浓度/mol•L-1 | c1 | c2 |
| CO2 的体积分数 | V1 | V2 |
| 体系的压强(Pa) | p1 | p2 |
| 气态反应物的转化率 | α1 | α2 |
| A. | 2c1=3c2 | B. | V1=V2 | C. | p1=p2 | D. | α1=α2 |
分析 Fe(s)+CO2(g)?FeO(s)+CO(g),反应是气体体积不变的吸热反应,依据图表数据分析,反应前后气体体积不变,加入2molCO2,加入3mol CO,相当于加入3molCO2,的平衡状态,气体物质条件分数相同,物质的量不同,压强不同,气体物质的量大的容器中压强大,起始量不同,平衡浓度、转化率不同.
解答 解:依据图表数据分析,反应前后气体体积不变,加入2molCO2,加入3mol CO,相当于加入3molCO2,平衡时气体体积分数相同,物质的量不同,压强不同,气体物质的量大的容器中压强大,起始量不同,平衡浓度、转化率不同;
A.达到平衡状态,一氧化碳的浓度关系为:3c1=2c2,故A错误;
B.反应物和生成物都是一种,平衡常数相同,所以达到平衡状态二氧化碳的体积分数相同,V1=V2,故B正确;
C.乙容器中气体物质的量大于甲容器,所以达到平衡状态p1<p2,故C错误;
D.起始量不同,甲容器正向进行,乙容器逆向进行,反应前后气体体积不变,气态反应物的转化率不相同,故D错误;
故选:B
点评 本题考查化学平衡影响因素、等效平衡、化学平衡的计算分析,难度中等,关键是构建平衡建立的等效途径.


科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①③ | C. | ①④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -2 | B. | +2 | C. | +4 | D. | +6 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;肼含有的化学键的种类与过氧化氢中完全一样,由此可以推论肼的结构式为
;肼含有的化学键的种类与过氧化氢中完全一样,由此可以推论肼的结构式为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②③ | C. | ②④ | D. | ② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
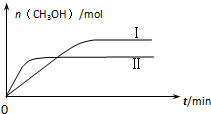 研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义.
研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义.| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2、3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com