
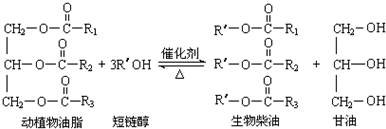
| A. | “地沟油”可用于制备生物柴油 | B. | 生物柴油属于油脂 | ||
| C. | 该反应属于酯化反应 | D. | 生物柴油的氧化反应是吸热反应 |
分析 A、“地沟油”中含有动植物油脂,根据题干信息来分析;
B、油脂是高级脂肪酸的甘油酯;
C、酸和醇反应生成酯和水的反应为酯化反应;
D、生物柴油的氧化反应即为燃烧反应.
解答 解:A、“地沟油”中含有动植物油脂,而动植物油脂与醇反应可制备生物柴油,故地沟油可以制备生物柴油,故A正确;
B、油脂是高级脂肪酸的甘油酯,而生物柴油是酯类,但甘油酯,故不是油脂,故B错误;
C、酸和醇反应生成酯和水的反应为酯化反应,此反应不符合酯化反应的概念,故不是酯化反应,故C错误;
D、生物柴油的氧化反应即为燃烧反应,而所有的燃烧均为放热反应,故生物柴油的氧化反应为放热反应,故D错误.
故选A.
点评 本题主要考查了油脂的性质与用途,熟悉油脂结构及性质是解题关键,注意酯化反应的实质是酸和醇反应生成酯和水,题目难度不大.


科目:高中化学 来源: 题型:解答题
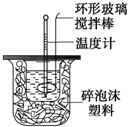 利用如图装置测定中和热的实验步骤如下:
利用如图装置测定中和热的实验步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.06 mol/(L•s) | B. | 1.8mol/(L•s) | C. | 1.2 mol/(L•s) | D. | 0.18 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、纤维素、蛋白质都是天然高分子化合物,都能发生水解反应 | |
| B. | 蔗糖和葡萄糖不是同分异构体,但属同系物 | |
| C. | 苯酚、甲醛通过加聚反应可制得酚醛树脂 | |
| D. | 石油裂解和煤的干馏都是化学变化,而石油的分馏和煤的气化都是物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴苯的制备: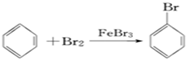 | |
| B. | 1,3-戊二烯发生加聚反应 | |
| C. | 苯酚钠溶液中通入少量二氧化碳: | |
| D. | 醇可以制备卤代烃,如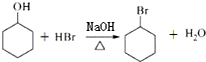 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子由锌经导线流向Ag2O | |
| B. | 负极的电极反应为Zn-2e-═Zn2+ | |
| C. | 溶液中OH-向正极移动 | |
| D. | 随着电极反应的不断进行,电解质的碱性减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 现象 | 结论 | |
| A | 食醋浸泡水垢 | 产生无色气体 | 乙酸的酸性比碳酸强 |
| B | 乙醇与橙色酸性重铬酸钾溶液混合 | 橙色溶液变为绿色 | 乙醇具有还原性 |
| C | 碘酒滴到土豆片上 | 土豆片变蓝 | 淀粉遇碘变蓝 |
| D | 向甲苯中滴入适量浓溴水,振荡,静置 | 溶液上层呈橙红色,下层几乎无色 | 甲苯和溴发生取代反应,使溴水褪色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaClO3在反应中失去电子 | |
| B. | Na2SO3在反应中被还原为Na2SO4 | |
| C. | 在该反应中,NaClO3和Na2SO3的物质的量之比为2:1 | |
| D. | 1 mol NaClO3参加反应有2 mol 电子转移 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com