
| 元素 | 相关信息 |
| A | 该元素的一种核素无中子 |
| B | 基态原子核外只有三个能级,且各能级电子数相等 |
| C | 基态原子最外层电子数是其内层电子总数的2.5倍 |
| D | 一个D-离子含18个电子 |
| E | +3价离子3d能级为半充满 |
 .
. ,C的氢化物在同族元素中氢化物的沸点出现反常,其原因是NH3分子间易形成氢键.
,C的氢化物在同族元素中氢化物的沸点出现反常,其原因是NH3分子间易形成氢键.分析 常见元素A、B、C、D、E的原子序数依次增大,A元素的一种核素无中子,则A为H元素;B的基态原子核外只有三个能级,且各能级电子数相等,则B原子核外电子排布为1s22s22p2,则B为C元素;C的基态原子最外层电子数是其内层电子总数的2.5倍,则C原子核外有2个电子层,最外层电子数为5,则C为N元素;D的一个D-离子含18个电子,则D原子核外电子总数=核电荷数=17,为Cl元素;E3+的3d能级为半充满,其基态原子的电子排布式为:1s22s22p63s23p63d64s2或[Ar]3d64s2,为Fe元素,
根据以上分析进行解答.
解答 解:常见元素A、B、C、D、E的原子序数依次增大,A元素的一种核素无中子,则A为H元素;B的基态原子核外只有三个能级,且各能级电子数相等,则B原子核外电子排布为1s22s22p2,则B为C元素;C的基态原子最外层电子数是其内层电子总数的2.5倍,则C原子核外有2个电子层,最外层电子数为5,则C为N元素;D的一个D-离子含18个电子,则D原子核外电子总数=核电荷数=17,为Cl元素;E3+的3d能级为半充满,其基态原子的电子排布式为:1s22s22p63s23p63d64s2或[Ar]3d64s2,为Fe元素,
(1)E为Fe元素,其基态核外电子排布式为:1s22s22p63s23p63d64s2,铁元素位于第4周期第VIII族,故答案为:第4周期第VIII族;
(2)N原子核外有7个电子,分别位于1S、2S、2P轨道,其轨道表示式为 ,故答案为:
,故答案为: ;
;
(3)氮气的电子式为 ,由于氨分子间存在氢键,故使其沸点出现反常,故答案为:
,由于氨分子间存在氢键,故使其沸点出现反常,故答案为: ;NH3分子间易形成氢键;
;NH3分子间易形成氢键;
(4)D的氢化物为HCl,其最高价氧化物的水化物的钾盐为KClO4,共热能发生反应,生成一种气体单质,应为Cl2,反应的方程式为:8HCl+KClO4$\frac{\underline{\;\;△\;\;}}{\;}$KCl+4Cl2↑+4H2O,
故答案为:8HCl+KClO4$\frac{\underline{\;\;△\;\;}}{\;}$KCl+4Cl2↑+4H2O;
(5)由A、B两种元素组成的含4个原子的非极性分子为乙炔,直线型sp杂化;13g乙炔的燃烧完全燃烧放出的热量为600kj,所以乙炔的燃烧热为1200kJ∕mol,则乙燃烧热的热化学反应方程式为C2H2(g)+$\frac{5}{2}$O2(g)=2CO2(g)+H2O(l)△H=-1200 kJ/mol,故答案为:sp杂化;C2H2(g)+$\frac{5}{2}$O2(g)=2CO2(g)+H2O(l)△H=-1200 kJ/mol.
点评 本题考查结构性质位置关系应用,题目难度中等,涉及元素在周期表中的位置、电子式等知识,注意掌握原子结构与元素周期表、元素周期律的关系.


科目:高中化学 来源: 题型:解答题
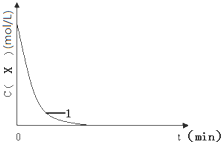 件下进行):
件下进行):| 编号 | 往烧杯中加入的试剂及其用量(mL) | 催化剂 | 开始变蓝时间(min) | ||||
| 0.1 mol•Lˉ1 KI溶液 | H2O | 0.01 mol•Lˉ1 X 溶液 | 0.1 mol•Lˉ1 双氧水 | 1 mol•Lˉ1 稀盐酸 | |||
| 1 | 20.0 | 10.0 | 10.0 | 20.0 | 20.0 | 无 | 1.4 |
| 2 | 20.0 | m | 10.0 | 10.0 | n | 无 | 2.8 |
| 3 | 10.0 | 20.0 | 10.0 | 20.0 | 20.0 | 无 | 2.8 |
| 4 | 20.0 | 10.0 | 10.0 | 20.0 | 20.0 | 5滴Fe2(SO4)3 | 0.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
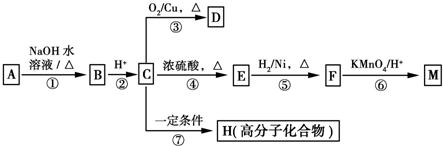
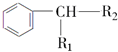 $→_{H+}^{KMnO_{4}}$
$→_{H+}^{KMnO_{4}}$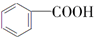 (R1、R2表示烃基或氢原子)
(R1、R2表示烃基或氢原子)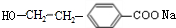 .
.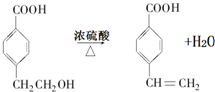 .
.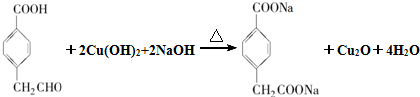 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相对分子质量相同,组成元素也相同的化合物一定是同分异构体 | |
| B. | 凡是分子组成相差一个或若干个CH2原子团的物质,彼此一定是同系物 | |
| C. | 两种物质的组成元素相同,各元素的质量分数也相同,则两者一定是同分异构体 | |
| D. | 分子式相同的不同有机物一定互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -488.3 kJ/mol | B. | -244.15 kJ/mol | C. | 488.3 kJ/mol | D. | 244.15 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、Cl-、Fe2+、Ba2+ | B. | OH-、NO3-、Ba2+、Cl- | ||
| C. | H+、CO32-、Mg2+、Ba2+ | D. | OH-、NO3-、CO32-、Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硝酸和过量的铁屑反应:Fe+4H++NO3-═Fe3++NO↑+2H2O | |
| B. | NH4HCO3溶液与少量的NaOH溶液混合:HCO3-+OH-═CO32-+H2O | |
| C. | 碳酸氢钠溶液水解的离子方程式:HCO3-+H2O?CO32-+H3O+ | |
| D. | Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Ba2+、Cl-、AlO2- | B. | SO42-、NO3-、Fe2+、Al3+ | ||
| C. | Cl-、SO32-、Na+、K+ | D. | Na+、K+、ClO-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/S | 0 | 1 | 2 | 3 | 4 | 5 |
| C(NO)(×10-4mol•L-1) | 10.0 | 4.05 | 2.50 | 1.50 | 1.00 | 1.00 |
| C(CO) (×10-3mol•L-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
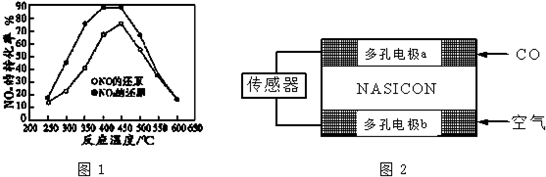
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com