
| A. | NaHCO3 | B. | NH4C1 | C. | KNO3 | D. | CH3COONa |
分析 根据盐类水解规律”谁强谁显性、谁弱谁水解、强强显中性”来确定这四种盐溶液的酸碱性,盐类水解规律:强酸弱碱盐水解显酸性;强碱弱酸盐水解显碱性;强酸强碱盐显中性,据此分析解答.
解答 解:A.NaHCO3溶液呈碱性原因是碳酸氢根离子水解生成氢氧根离子,离子方程式:HCO3-+H2O?H2CO3+OH-,故A错误;
B.氯化铵为强酸弱碱盐,水解呈酸性,铵根离子水解的离子方程式为NH4++H2O?H++NH3•H2O,故B错误;
C.KNO3为强酸强碱盐,不水解,溶液呈中性,故C正确;
D.CH3COONa强碱弱酸盐,水解离子反应为CH3COO-+H2O?CH3COOH+OH-,则溶液显碱性,故D错误;
故选C.
点评 本题考查了盐溶液酸碱性判断,根据盐的类型及盐中发生水解反应的离子来确定溶液酸碱性,盐类水溶液酸碱性强弱与弱离子水解程度有关,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 55% | B. | 60% | C. | 65% | D. | 70% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
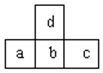
| A. | d的氢化物比b的氢化物稳定 | |
| B. | d与c不能形成化合物 | |
| C. | a、b、c的最高价氧化物对应水化物的酸性强弱的关系是c>b>a | |
| D. | 原子半径的大小顺序是a>b>c>d |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 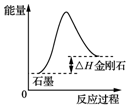 由图可知,从能量角度考虑,金刚石比石墨稳定 | |
| B. | 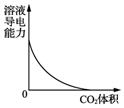 图表示CO2通入饱和Na2CO3溶液中,溶液导电能力的变化 | |
| C. | 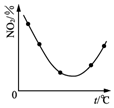 图表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)?N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0 | |
| D. | 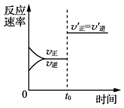 图表示某可逆反应的反应速率随时间的变化,t0时刻改变的条件一定是使用了催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖类和蛋白质都属于高分子化合物 | B. | 苯和聚乙烯均能发生加成反应 | ||
| C. | C5H11Cl有6种同分异构体 | D. | 石油分馏、煤干馏都可得到烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业制漂白粉:C12+2OH-═Cl-+ClO-+H2O | |
| B. | 将氯气溶于水制备次氯酸:C12+H2O═2H++Cl-+ClO- | |
| C. | 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+ | |
| D. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Y | Z | ||
| R |
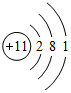 ;R在周期表中的位置为第三周期ⅢA族.
;R在周期表中的位置为第三周期ⅢA族.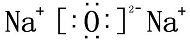 ,Q2Z2含的化学键类型为:离子键、共价键.
,Q2Z2含的化学键类型为:离子键、共价键.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
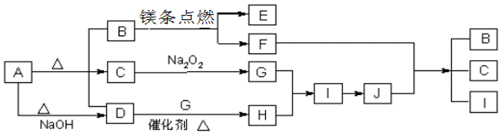
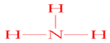 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 容器编号 | 起始时各物质物质的量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ | |||
| CO | H2O | CO2 | H2 | |||
| ① | 1 | 4 | 0 | 0 | t1 | 放出热量:32.8 kJ |
| ② | 2 | 8 | 0 | 0 | t2 | 放出热量:Q |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com