
 ,A→C的反应类型:加成反应.
,A→C的反应类型:加成反应.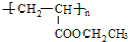 ,写出D的同分异构体的结构简式:CH3OCH3.
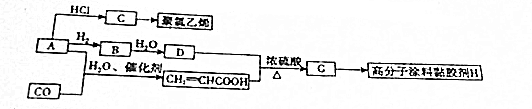
,写出D的同分异构体的结构简式:CH3OCH3.分析 A与HCl反应的生成物C能够制取聚氯乙烯,可知A为CH≡CH,乙炔与HCl通过加成反应生成的C为CH2=CHCl,C发生加聚反应得到聚氯乙烯.乙炔与氢气发生加成反应生成B为CH2=CH2,乙烯水化生成的D为CH3CH2OH,乙醇与CH2=CHCOOH发生酯化反应生成的G为CH2=CHCOOCH2CH3,G通过加聚反应生成高分子涂料H为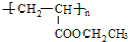 .乙炔与CO、水反应加成反应得到CH2=CHCOOH.
.乙炔与CO、水反应加成反应得到CH2=CHCOOH.
解答 解:A与HCl反应的生成物C能够制取聚氯乙烯,可知A为CH≡CH,乙炔与HCl通过加成反应生成的C为CH2=CHCl,C发生加聚反应得到聚氯乙烯.乙炔与氢气发生加成反应生成B为CH2=CH2,乙烯水化生成的D为CH3CH2OH,乙醇与CH2=CHCOOH发生酯化反应生成的G为CH2=CHCOOCH2CH3,G通过加聚反应生成高分子涂料H为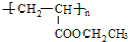 .乙炔与CO、水反应加成反应得到CH2=CHCOOH.
.乙炔与CO、水反应加成反应得到CH2=CHCOOH.
(1)A为CH≡CH,电子式为 ,A为CH≡CH,乙炔与HCl通过加成反应生成的C为CH2=CHCl,
,A为CH≡CH,乙炔与HCl通过加成反应生成的C为CH2=CHCl,
故答案为: ;加成反应;
;加成反应;
(2)H的结构简式: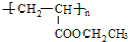 ,D为CH3CH2OH,D的同分异构体的结构简式:CH3OCH3,
,D为CH3CH2OH,D的同分异构体的结构简式:CH3OCH3,
故答案为: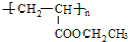 ;CH3OCH3;
;CH3OCH3;
(3)生成G的化学方程式:CH2=CHCOOH+CH3CH2OH$→_{△}^{浓硫酸}$CH2=CHCOOCH2CH3+H2O,
故答案为:CH2=CHCOOH+CH3CH2OH$→_{△}^{浓硫酸}$CH2=CHCOOCH2CH3+H2O;
(4)若要除去甲烷中混有的B(乙烯)气体,可将混合气体通入酸性高锰酸钾溶液中,D可由葡萄糖在酶的作用下产生,葡萄糖属于还原性糖,而蔗糖不是还原性糖,若要鉴别葡萄糖与蔗糖可选用的化学试剂是:新制的氢氧化铜浊液,
故答案为:酸性高锰酸钾溶液;新制的氢氧化铜浊液;
(5)D(乙醇)也可由有机物C4H8O2在氢氧化钠溶液加热的条件下生成,是乙酸乙酯发生水解反应,该反应的化学方程式:CH3COOCH2CH3+NaOH$\stackrel{△}{→}$CH3COONa+CH3CH2OH,
故答案为:CH3COOCH2CH3+NaOH$\stackrel{△}{→}$CH3COONa+CH3CH2OH.
点评 本题考查有机物的推断,注意根据有机物的结构进行推断,需要学生熟练掌握官能团的性质与转化,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 卤代烃中卤原子的检验:先加NaOH溶液、加热、冷却后加AgNO3溶液 | |
| B. | 乙烷中有乙烯可KMnO4溶液洗气,除去杂质 | |
| C. | 碳原子数小于10,且一氯代物只有一种的烷烃有3种 | |
| D. | 可用水鉴别苯和四氯化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不能自发进行的氧化还原反应,通过电解的原理可以实现 | |
| B. | 电镀时保持电流恒定,升高温度不改变电解反应速率 | |
| C. | 电解精炼铜电解槽底部会形成含少量Ag、Fe、Pt等金属的阳极泥 | |
| D. | 氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 | |
| E. | MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液,若电解电路中通过2mol电子,MnO2的理论产量为1mol | |
| F. | 燃料电池是将燃料燃烧所放出的能量转化为化学能的装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2+X2═2HX | B. | X2+H20═HX+HXO | ||
| C. | NaX+AgNO3═AgX↓+NaNO3 | D. | 2NaX+H2SO4(浓)═Na2SO4+2HX |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2>Fe3+>Cu2+>PbO2 | B. | PbO2>Cl2>Fe3+>Cu2+ | ||
| C. | Fe3+>Cu2+>PbO2>Cl2 | D. | Cu2+>Fe3+>Cl2>PbO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
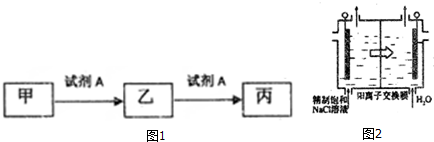
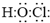 .二氧化氯还能溶于强碱溶液,该过程中发生反应生成等物质的量的氯酸钠(NaClO3)和另一种氯的含氯酸盐,同时生成水,该反应的离子方程式为2ClO2+2OH-═ClO3-+ClO2-+H2O
.二氧化氯还能溶于强碱溶液,该过程中发生反应生成等物质的量的氯酸钠(NaClO3)和另一种氯的含氯酸盐,同时生成水,该反应的离子方程式为2ClO2+2OH-═ClO3-+ClO2-+H2O查看答案和解析>>
科目:高中化学 来源: 题型:解答题
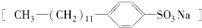 是常用洗涤剂的主要成分.其结构可用图形
是常用洗涤剂的主要成分.其结构可用图形 来表示,•端为链烃基,O端为极性基.根据这一结构特点,试分析和回答下列问题:
来表示,•端为链烃基,O端为极性基.根据这一结构特点,试分析和回答下列问题: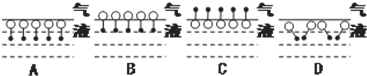
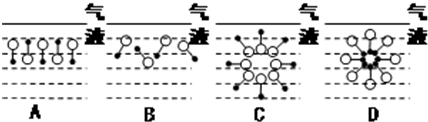
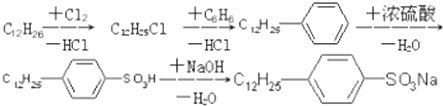
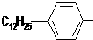 .
.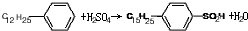 ,反应类型为取代反应.
,反应类型为取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不同元素的原子发生跃迁时,会释放不同的光 | |
| B. | 第一电离能与电负性的数值都是以气态中性基态原子为研究对象测得到 | |
| C. | 分子中的原子有固定的空间位置,组成完全相同的分子,由于原子位置的不同会表现出不同的性质 | |
| D. | 两个相同的原子的任意未成对电子的电子云在两个原子核间重叠,形成非极性共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com