
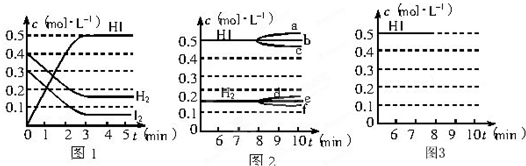
ŌŚÄ³Ņ»ČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÄŚ£¬¼ÓČė0.8 mol µÄH2ŗĶ0.6 mol µÄI2 £»ŌŚŅ»¶ØµÄĢõ¼žĻĀ·¢ÉśČēĻĀ·“Ó¦£ŗH2(g) £« I2(g) ![]() 2HI(g) £« Q(Q£¾0)”£·“Ó¦ÖŠø÷ĪļÖŹµÄÅضČĖꏱ¼ä±ä»ÆĒéæöČēĶ¼1£ŗ
2HI(g) £« Q(Q£¾0)”£·“Ó¦ÖŠø÷ĪļÖŹµÄÅضČĖꏱ¼ä±ä»ÆĒéæöČēĶ¼1£ŗ

¢Åøł¾ŻĶ¼1Źż¾Ż£¬·“Ó¦æŖŹ¼ÖĮ“ļµ½Ę½ŗāŹ±£¬Ę½¾łĖŁĀŹV£ØHI£©ĪŖ___________”£
(¾«Č·µ½Š”ŹżµćŗóµŚ3Ī»)
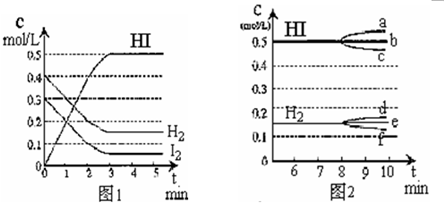
¢Ę·“Ó¦“ļµ½Ę½ŗāŗ󣬵Ś8·ÖÖÓŹ±£¬ČōÉżøßĪĀ¶Č£¬ HIÅØ¶ČµÄ±ä»ÆÕżČ·µÄŹĒ___________£ØÓĆĶ¼2ÖŠa~cµÄ±ąŗÅ»Ų“š£©”£
¢Ē·“Ó¦“ļµ½Ę½ŗāŗ󣬵Ś8·ÖÖÓŹ±£¬Čō¼ÓČėI2, ŌņH2ÅØ¶ČµÄ±ä»ÆÕżČ·µÄŹĒ___________£ØÓĆĶ¼2ÖŠd~fµÄ±ąŗÅ»Ų“š£©”£
¢Č·“Ó¦“ļµ½Ę½ŗāŗ󣬵Ś8·ÖÖÓŹ±£¬Čō°ŃČŻĘ÷µÄČŻ»żĄ©“óŅ»±¶£¬ĒėŌŚĶ¼ÖŠ»³ö“ÓµŚ8·ÖÖÓæŖŹ¼ĻņŗóHIÅØ¶ČµÄ±ä»ÆĒéæö”£ks5u

 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| c2(HI) |
| c(H2)c(I2) |
| c2(HI) |
| c(H2)c(I2) |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
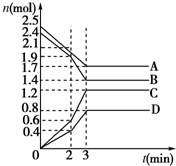 ŌŚÄ³Ņ»ČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ£¬A”¢B”¢C”¢DĖÄÖÖĪļÖŹµÄĪļÖŹµÄĮæn£Ømol£©Ėꏱ¼ät£Ømin£©µÄ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£ŗ
ŌŚÄ³Ņ»ČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ£¬A”¢B”¢C”¢DĖÄÖÖĪļÖŹµÄĪļÖŹµÄĮæn£Ømol£©Ėꏱ¼ät£Ømin£©µÄ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| c2(HI) |
| c(H2)c(I2) |
| c2(HI) |
| c(H2)c(I2) |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com