

��2������ƿ�ռ������CO2����ƿ����һֻ�����ڲ�����ĩ�˵�С������ͼ��ʾ��

�ٴ�ƿ����Ѹ�ٷֱ�����������ʣ�����������һ��ʱ���������Զ����͵���________������ţ���
A��Na2O �������������������� B��Na2O2
C��Na2CO2 �������������������� D��NaOH
������ƿ��װ��10mLH2O��������CO2������һ�����Ľ����ƺ�Ѹ������ƿ�����Ը���������״�ı仯����������Һ�����ʵĿ�����ɡ�

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
(1)���Ҵ��ķе��ʵ��Ҫ�������Ҵ�������99.5����ʵ����ֻ��95.6�����Ҵ���������Ҫ�Ʊ���ˮ�Ҵ���ʵ�����Ʊ���ˮ�Ҵ���ԭ�������Ҵ�95.6%��ˮ4.4%���һ�ֻ�����ѹ�£�����һ���ķе�(78.17 ��)������е�ȵ���ˮ�ķе�(100 ��)Ҳ�����Ҵ��ķе�(78.3 ��)������ֻ��������ƾ������Ҵ��������ֻ�ܴﵽ95.6%���к���4.4%��ˮ�����Ҫ�õ������ϸߵ��Ҵ�����ʵ�����г��õļ�㷽���Ǽ�����ʯ�һ���(��������һ�����Լ��ȵķ�Ӧ�����У���Һ�����ʹ����ת�����ɵ�����ͨ�������������ֻ�����ԭ�����IJ�����(��ͼ��)������֮�������ɵ�99.5%���Ҵ���ͨ����Ϊ��ˮ�Ҵ������Ҫ�õ����ȸ��ߵľ����Ҵ�(���Ҵ�99.95%)����Ҫ�ý����ƽ��д��������Գ�ȥ�������ˮ�֡�
ʵ�鲽�裺ȡ�����250 mLԲ����ƿһֻ������95.6%�Ҵ�100 mL��С����ʯ��30 g����ҡ������Ƥ�����������ù�ҹ������ƿ��װ�ϻ��������ܣ��ܿڽ�һ֧��ˮ�Ȼ��Ƹ����(װ�ü�ͼ��)����ˮԡ�ϼ��Ȼ���1��2Сʱ�����䣬ȡ�������ܣ���װ������װ��(��ͼ��)���ٷ�����ˮԡ���������������5 mL���Һ������գ�Ȼ���ú�ɵ�����ƿ��Ϊ�����������ܽ�һ֧�Ȼ��Ƹ���ܣ�ʹ���������ͨ��������Һ�γ���Ϊֹ��

������������⣺
��Ϊʲô���ջ������Ҵ�ʱ��Ҫװ����ˮ�Ȼ��Ƹ���ܣ�
____________________________________________________________________
____________________________________________________________________��
����ͼ����ʾ����ˮ�Ҵ�������װ��������ˮ��__________������__________������
����ͼ����ʾװ����Ϊ�˷�ֹ����ϵͳ�ⲿʪ�����룬���������Ӱ��������϶�������������Ϊʲô���У�____________________________________________________________��

�ⶨ�е�ļ���װ��
(2)���Ƶõ���ˮ�Ҵ���������ͼ��ʾ��װ���н��зе�ⶨ��ʵ�飬����������⣺
��ʢ�Ҵ����Թ�Ӧ����ˮԡ�У�ˮԡ���¶�Ӧ������__________��
A.100 �� B.78.5 �� C.80 �� D.50 ��
�ڲ��Ҵ��е�ʱΪʲô���������Թܽ���ˮ�Ϊʲô������Ҫ�и����ڣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
��14�֣���ҵ��һ���ں����ܱ������п��Բ������з�Ӧ�ϳɼ״���
��1���жϷ�Ӧ�ﵽƽ��״̬�������ǣ�����ĸ��ţ���ͬ��__________��
A. ����������������
���������
B. ���������ܶȲ���
C. �����������ƽ��������������
D. ��
��
��Ũ�ȶ����ٷ����仯
E. �����ѹǿ���ٸı�
��2���±����������Ƿ�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
���ɱ��������жϸ÷�Ӧ�ġ�H__________0���>������=����<������
��ij�¶��£�����
����
���ܱ������У���ַ�Ӧ�ﵽƽ��ʱ���
����CO��ת����Ϊ__________����ʱ���¶�Ϊ__________��
��3��Ҫ���CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ��__________��
a. ���� b. ������� c.����CO��Ũ��
d. �����¼��� ʹѹǿ��� e. �����¼����������ʹѹǿ��� f. ������״�
��4����250��ʱ��ijʱ�̲�ø��¶��µ��ܱ������и����ʵ����ʵ���Ũ�ȼ��±�:
| CO | | |
| 0.5 mol��L��1 | 2mol��L��1 | 6mol��L��1 |
��ʱ��Ӧ�������淴Ӧ���ʵĹ�ϵ�ǣ�v������ v���棩������ڡ���С�ڡ����ڡ�����
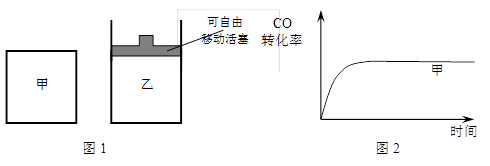
��5����ͼ1��ʾ����Ϊ�����ܱ���������Ϊ��ѹ�ܱ��������ڼס����������зֱ��������ʵ�����H2��CO��ʹ�ס�����������ʼ�ݻ���ȡ�����ͬ�¶��·���������Ӧ����ά�ַ�Ӧ�������¶Ȳ��䡣��֪��������CO��ת������ʱ��仯��ͼ����ͼ2��ʾ������ͼ2�л�����������CO��ת������ʱ��仯��ͼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ�꽭��ʡЭ���������һ���������ۻ�ѧ�Ծ��������棩 ���ͣ������
2013��ȫ�����ض�������ʮ�������������У�������β����ȼú�����������Կ����������ϴ�
��1������β����������Ҫԭ��Ϊ��2NO(g) + 2CO(g) 2CO2(g)+ N2(g)����H��0
2CO2(g)+ N2(g)����H��0
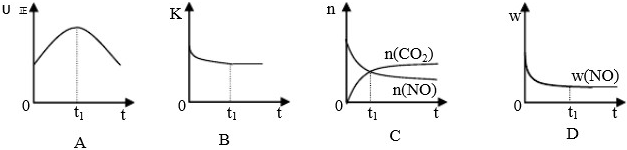
���÷�Ӧ�ھ��ȡ����ݵ��ܱ���ϵ�н��У�����ʾ��ͼ��ȷ����˵����Ӧ�ڽ��е�t1ʱ�̴ﵽƽ��״̬����???????? ������ţ���
����ͼ��������K��n��w�ֱ��ʾ����Ӧ���ʡ�ƽ�ⳣ�������ʵ���������������

��2��������β����úȼ�ղ����������������������CH4����ԭNOX�������������������Ⱦ����֪��CH4(g)+2NO2(g)��N2(g)��CO2(g)+2H2O(g)? ��H����867 kJ/mol
2NO2(g) N2O4(g)?? ��H����56.9 kJ/mol
N2O4(g)?? ��H����56.9 kJ/mol
H2O(g) �� H2O(l)?? ��H �� ��44.0 kJ��mol
д��CH4����ԭN2O4(g)����N2��H2O(l)���Ȼ�ѧ����ʽ��???????????????????????????????????? ��
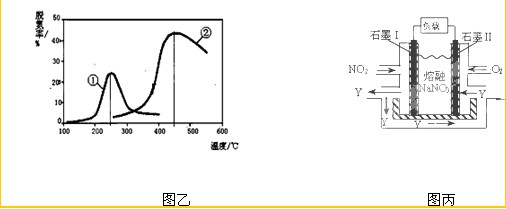
��3����NH3����ԭNOXҲ�������������������Ⱦ����ͼ������NH3����ԭ����������һ��������ͨ�����ֲ�ͬ�����������ݳ������е������ﺬ�����Ӷ�ȷ�������ѵ��ʣ�ע���ѵ��ʼ���������ת���ʣ���
��Ӧԭ��Ϊ��NO(g) +NO2(g)+2NH3(g) 2N2(g) + 3H2O(g)��
2N2(g) + 3H2O(g)��

���÷�Ӧ����S???? 0����H????? 0�������������������� ����������
���������巴Ӧ����ij���(B)��ƽ��ѹǿ(pB)�������ʵ���Ũ��(cB)Ҳ���Ա�ʾƽ�ⳣ��������KP����
��������Ӧ��KP��???????????????? ��
������˵����ȷ����????????????????? ��
A�������ִ����ȵ����ִ����ѵ��ʸ�
B����ͬ�����£��ı�ѹǿ���ѵ���û��Ӱ��
C�������������ֱ��ʺ���250����450�������ѵ�
��4��NO2��O2������NaNO3������ȼ�ϵ�أ���ԭ����ͼ���õ����ʹ�ù�����ʯīI�缫������������Y����缫��ӦΪ?? ??????????????????? ? ��

��5�����Ṥҵβ���е������NO��NO2������������CO(NH2)2����Һ��ȥ����Ӧ���ɶԴ�������Ⱦ�����塣1 mol���������չ�ҵβ���е����������NO��NO2�����Ϊ1:1��������Ϊ___________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�츣��ʡ�����и߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
��ҵ��һ���ں����ܱ������п��Բ������з�Ӧ�ϳɼ״���
CO(g) + 2H2(g)  CH3OH(g)
CH3OH(g)
��1���жϷ�Ӧ�ﵽƽ��״̬�������ǣ�����ĸ��ţ���ͬ��__________��
A������CH3OH������������CO���������
B�����������ܶȲ���
C�������������ƽ��������������
D��CH3OH��CO��H2��Ũ�ȶ����ٷ����仯
E. �����������ѹǿ���ٸı�
��2���±����������Ƿ�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
|
�¶� |
250�� |
300�� |
350�� |
|
K |
2.041 |
0.270 |
0.012 |
���ɱ��������жϸ÷�Ӧ�ġ�H__________0���>������="��" ��<������
��ij�¶��£���2 mol CO��6 mol H2����2L���ܱ������У���ַ�Ӧ�ﵽƽ��ʱ���c(CO) =" 0.2" mol/L����CO��ת����Ϊ__________����ʱ���¶�Ϊ__________��
��3��Ҫ���CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ��__________��
a. ���� b. �������
c. ����CO��Ũ�� d. �����¼���H2ʹ������ѹǿ���
e. ������״� f. �����¼����������ʹ������ѹǿ���
��4����250��ʱ��ijʱ�̲�ø��¶��µ��ܱ������и����ʵ����ʵ���Ũ�ȼ��±�:
|
CO |
H2 |
CH3OH |
|
0.5 mol��L-1 |
2mol��L-1 |
6mol��L-1 |
��ʱ��Ӧ�������淴Ӧ���ʵĹ�ϵ�ǣ�v������ v���棩���>������="��" ��<������
��5����ͼ1��ʾ����Ϊ�����ܱ���������Ϊ��ѹ�ܱ��������ڼס����������зֱ��������ʵ�����H2��CO��ʹ�ס�����������ʼ�ݻ���ȡ�����ͬ�¶��·���������Ӧ����ά�ַ�Ӧ�������¶Ȳ��䡣��ͼ2�б���ס�����������CO��ת������ʱ��仯�Ķ�Ӧͼ��(��ͼ����Ӧ�����Ҳ�Ŀ���зֱ��ע���ס������ҡ�)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com