
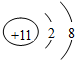 ��
������ A��B��C��D��E�Ƕ����ڵ�����Ԫ�أ�����ԭ��������������AԪ����Ԫ�����ڱ���ԭ�Ӱ뾶��С����AΪHԪ�أ�C��D��E����Ԫ�ص�����������Ӧˮ����֮�����������Ӧ��Ӧ������������ǿ�ᡢǿ��֮��ķ�Ӧ����DΪAl��A��Cͬ���壬��CΪNa��E�ĵ���Ϊ����ɫ���壬��Ȼ��������̬��E�������ڻ�ɽ�ڸ�������EΪS��B��Eͬ���壬��BΪOԪ�أ��ݴ˽��
��� �⣺A��B��C��D��E�Ƕ����ڵ�����Ԫ�أ�����ԭ��������������AԪ����Ԫ�����ڱ���ԭ�Ӱ뾶��С����AΪHԪ�أ�C��D��E����Ԫ�ص�����������Ӧˮ����֮�����������Ӧ��Ӧ������������ǿ�ᡢǿ��֮��ķ�Ӧ����DΪAl��A��Cͬ���壬��CΪNa��E�ĵ���Ϊ����ɫ���壬��Ȼ��������̬��E�������ڻ�ɽ�ڸ�������EΪS��B��Eͬ���壬��BΪOԪ�أ�
��1��������������֪��AΪ�⣬EΪ��Ԫ��E��Ԫ�����ڱ��е�λ���ǣ��������ڵ�VIA�壬
�ʴ�Ϊ���⣻�������ڵ�VIA�壻
��2��CΪNaԪ�أ������ӽṹʾ��ͼΪ��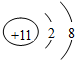 ���ʴ�Ϊ��
���ʴ�Ϊ��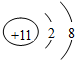 ��
��
��3��C��D������������Ӧˮ����ֱ�ΪNaOH��Al��OH��3�����߷�Ӧ����ƫ��������ˮ����Ӧ�Ļ�ѧ����ʽΪAl��OH��3+NaOH=NaAlO2+2H2O��
�ʴ�Ϊ��Al��OH��3+NaOH=NaAlO2+2H2O��
��4��H��O��Na����Ԫ���γɵĻ�����ΪNaOH���������Ӽ������ۼ����ʴ�Ϊ�����Ӽ������ۼ���
��5��ͬ������ԭ����������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶����ԭ�Ӱ뾶�ɴ�С������˳��ΪNa��Al��S��O���ʴ�Ϊ��Na��Al��S��O��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��ѶȲ����ƶ�Ԫ���ǽ���ؼ������ضԻ���֪ʶ�Ŀ��飬ע���������뾶�ıȽϹ��ɣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
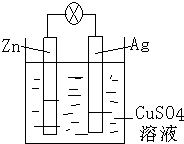 ��ѧ��Ӧ�����������ܲ��ɷֵĹ�ϵ���ش��������⣮
��ѧ��Ӧ�����������ܲ��ɷֵĹ�ϵ���ش��������⣮| ���� | H2 | CO | CH4 |
| ȼ���ȣ�kJ•mol-1�� | 285.8 | 283.0 | 890.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������̼���ӵĵ���ʽ��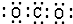 | B�� | HClO�ĽṹʽΪ H-Cl-O | ||
| C�� | ���ԭ�ӽṹʾ��ͼ��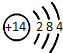 | D�� | ������ӵı���ģ�ͣ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SiO2��SO2�������������������NaOH��Һ��Ӧ | |
| B�� | Na2O��Na2O2���Ԫ����ͬ����CO2��Ӧ����Ҳ��ͬ | |
| C�� | CO��NO��NO2���Ǵ�����Ⱦ���壬�ڿ����ж����ȶ����� | |
| D�� | ����������Ư���ԣ�ͨ��������ɫʯ����Һ�У��������Һ��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����������м�����ǿ����NaOH | B�� | ���ʻ�ԭ������ǿ������ | ||
| C�� | �����۵���͵����� | D�� | ԭ�Ӱ뾶������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� ���� | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | E | R | F | |||||
| 3 | A | C | D | H | I | G | ||
| 4 | B |
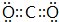 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1mol•L-1��NH4��2Fe��SO4��2��Һ��c ��SO42-����c��NH4+����c��Fe2+����c��H+�� | |
| B�� | ������pH=2��HCl��Һ��pH=12�İ�ˮ��Һ��������c��NH4+��=c��Cl-�� | |
| C�� | 0.2 mol•L-1 Na2CO3��Һ�У�2c��Na+��=c��CO32-��+c��HCO3-��+c��H2CO3�� | |
| D�� | ij��Ԫ�������ʽ��NaHA��Һ��c��Na+��+c��H+��=c��OH-��+c��HA-��+c��A2-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
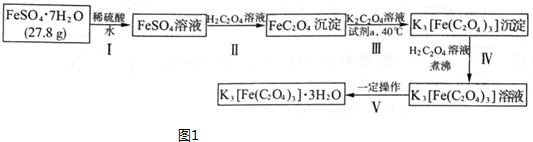
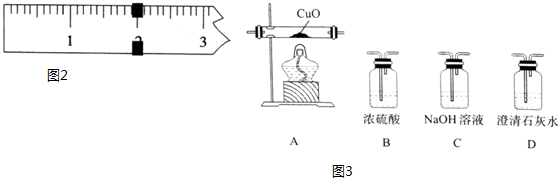
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com