
����Ŀ�����������¡����ݵ��ܱ������н��������������淴Ӧ��(��)2X(g)![]() Y(g)+Z(s)�� (��)A(s)+2B(g)
Y(g)+Z(s)�� (��)A(s)+2B(g)![]() C(g)+D(g)�����������������ٷ����仯ʱ�����Ա������Ҿ��ﵽƽ��״̬����
C(g)+D(g)�����������������ٷ����仯ʱ�����Ա������Ҿ��ﵽƽ��״̬����
�ٻ�������ܶ�
�ڷ�Ӧ������������İٷֺ���
�۷�Ӧ����������������������������֮�ȵ��ڻ�ѧ������֮��
�ܻ�������ѹǿ
�ݹ�������
�������������ʵ���
A���٢ڢۢܢݢ� B���٢ڢۢ� C���٢ڢ� D���ڢۢ�
���𰸡�B
��������
����������ټ��Ҿ��ɹ�����뷴Ӧ�����������ܶȲ��䣬����ƽ��״̬�ı�־����ѡ�� �ڷ�Ӧ������������İٷֺ�����˵������ֵ������䣬��ƽ��״̬����ѡ�� �۷�Ӧ����������������������������֮�ȵ���ϵ��֮�ȣ�˵�����淴Ӧ������ȣ���ѡ�����һ�������ѹǿʼ�ղ��䣬�ʲ�ѡ�� ��������������˵���������������ʲ��䣬����ƽ��״̬�ı�־����ѡ�� ���һ������������ʵ���ʼ�ղ��䣬�ʲ�ѡ�� ��ѡB��


 ������ÿ�ʱ�Ż���ҵϵ�д�
������ÿ�ʱ�Ż���ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ҫ���ں��ա�ұ��������ҵ������������һ�����������������̼���̿�(��Ҫ����FeS2��FeCO3��SiO2��CuO������)�Ʊ������̵Ĺ�����������:
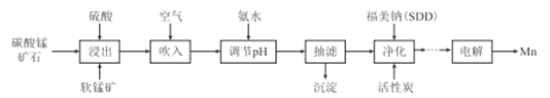
��֪:��.�����ƵĻ�ѧʽΪ(CH3)2CNS2Na,���ø����ƶ�MnSO4��Һ���ؽ������о���ȥ��Ч������:
��.���ֽ��������γ��������������pH���±���ʾ:
Fe2+ | Cu2+ | Fe3+ | Mn2+ | |
pH(��ʼ����) | 7.5 | 5.2 | 1.7 | 7.2 |
pH(��ȫ����) | 9.7 | 7.8 | 3.2 | 10.4 |
�ش���������:
��1��FeS2��SԪ�صĻ��ϼ�Ϊ_____�ۡ�
��2������ʱ�����̿��е���Ҫ�ɷ�MnO2��FeS2����������ԭ��Ӧ,д���÷�Ӧ�Ļ�ѧ����ʽ:___
��3�������Һ�д��������Ŀ����__________(�����ӷ���ʽ��ʾ)��
��4������pH����ѷ�Χ��_______,�����ijɷ���______(�ѧʽ)��
��5��(CH3)2CNS2H����(CH3)2NH��CS2ͨ���ӳɷ�Ӧ�õ�,1mol(CH3)2NH��,���ۼ�����ĿΪ__NA��
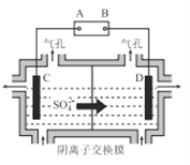
��6����ҵ�ϲ�����ͼ��ʾ�ķ�����ý���Mn��B��Ϊ____������û�������ӽ���Ĥ,Mn2+����D��������Ӧ����MnO2,��缫��ӦʽΪ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ���Ӧ��������������ǣ�������
A. ��ʾ1 LpH=2��CH3COOH��Һ��ˮϡ����V L��pH��lgV�ı仯
��ʾ1 LpH=2��CH3COOH��Һ��ˮϡ����V L��pH��lgV�ı仯
B. ��ʾ��ͬ�¶���ˮ��Һ��H+��OH��Ũ�ȵı仯�����ߣ�ͼ���¶�T2��T1
��ʾ��ͬ�¶���ˮ��Һ��H+��OH��Ũ�ȵı仯�����ߣ�ͼ���¶�T2��T1
C.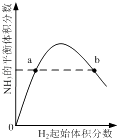 ��ʾһ�������µĺϳɰ���Ӧ�У�NH3��ƽ�����������H2��ʼ���������N2����ʼ���㶨���ı仯��ͼ��a��N2��ת����С��b��
��ʾһ�������µĺϳɰ���Ӧ�У�NH3��ƽ�����������H2��ʼ���������N2����ʼ���㶨���ı仯��ͼ��a��N2��ת����С��b��
D. ��ʾͬһ�¶��£��ڲ�ͬ�ݻ��������н��з�Ӧ2NO2��g��2NO��g��+O2��g����O2��ƽ��Ũ���������ݻ��Ĺ�ϵ
��ʾͬһ�¶��£��ڲ�ͬ�ݻ��������н��з�Ӧ2NO2��g��2NO��g��+O2��g����O2��ƽ��Ũ���������ݻ��Ĺ�ϵ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ڹ�ũҵ�����ж�����ҪӦ�á�
��1���£�N2H4���������ᷴӦ�����ɵ�����һ���⻯��ڱ�״���£����⻯��������ܶ�Ϊ1.92g/L�������е�Ԫ�ص���������Ϊ0.977����÷�Ӧ�Ļ�ѧ����ʽΪ____.
��2������������һ�������£����Է������·�Ӧ��SO2(g)+NO2(g)![]() SO3(g)+NO(g) ��H= -42kJ��mol-1����2L�ĺ����ܱ������г���SO2(g)��NO2(g)����ʵ���������£�
SO3(g)+NO(g) ��H= -42kJ��mol-1����2L�ĺ����ܱ������г���SO2(g)��NO2(g)����ʵ���������£�
ʵ���� | �¶� | ��ʼ���ʵ���mol | ƽ��ʱ���ʵ���/mol | |
n(SO2) | n(NO2) | n(NO) | ||
�� | T1 | 4.0 | 1.0 | 0.9 |
�� | T2 | 1.0 | 4.0 | 0.8 |
�� | T2 | 0.4 | 0.6 | a |
����ʵ����У���2minʱ��÷ų���������8.4kJ��0��2minʱ���ڣ���SO2��ʾ��ƽ����Ӧ����v(SO2)=_______________�����¶��µ�ƽ�ⳣ��Ϊ_________�������������С�������λ��
���ɱ������ݿ���֪��T1_______T2������>����<������=����
��ʵ����У��ﵽƽ��ʱNO2��ת����Ϊ______________.
��3����ҵ�Ͽ����ð�ˮ��SO2ת��ΪNH4HSO3����������(NH4)2SO4�������²��NH4HSO3��ҺpHΪ6������Һ��![]() ________________________.����֪��H2SO3��Kal =1.5��10-2Ka2 =1.0��10-7��
________________________.����֪��H2SO3��Kal =1.5��10-2Ka2 =1.0��10-7��
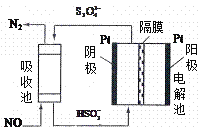
��4��ʹ�ü�ӵ绯ѧ�����Դ���ú�����е�NO��װ����ͼ����֪������Һ��pH��4��7֮�䣬д�������ĵ缫��Ӧʽ__________________��
 ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)�����¸����������ʣ�A.��������춡�顡B.���ʯ��ʯī��C60��C.���ɱ���D.35Cl��37Cl��E.NO��NO2�����У���Ϊͬ���칹�����__________(���ţ�����ͬ)����Ϊͬ�����������__________��
(2)���У��ٸɱ����ڽ��ʯ����NH4Cl����Na2S�������ʣ�������Ҫ��ش�(�����)���ۻ�ʱ����Ҫ�ƻ���ѧ������____________���ȴ������Ӽ��ִ��ڹ��ۼ�����____________��
(3)��һ���ݻ�Ϊ2 L���ܱ������г���7 mol SO2��4 mol O2����һ���¶Ⱥ�ѹǿ�£��������·�Ӧ��2SO2(g)��O2(g) 2SO3(g)����4 s��ﵽƽ��״̬�����SO2�����ʵ�����3 mol����ﵽƽ��״̬ʱO2��ת����Ϊ__________��ƽ��ʱSO3�����ʵ���Ũ��_______��
(4) NaBH4(s)��H2O(l)��Ӧ����NaBO2(s)����������25 �桢101 kPa�£���֪ÿ����3.8 g NaBH4(s)����21.6 kJ���÷�Ӧ���Ȼ�ѧ����ʽ��____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��DΪ������Ԫ�أ��˵��������������A��B��C����Ԫ�ص�ԭ�Ӻ�����Ӳ���֮��Ϊ5����֪A��ԭ�ӽṹ���Ԫ�أ�BԪ��ԭ��������ϵĵ�����������Ӳ�����2����A��C֮����γ�A2C��A2C2���ֻ����D��ͬ��������Ԫ����ԭ�Ӱ뾶�����ش��������⡣
(1)CԪ����Ԫ�����ڱ��е�λ����____________��C��D����Ԫ�����γɵļ����ӣ����Ӱ뾶�ɴ�С��˳����________________��(�����ӷ��ű�ʾ)
(2)д��A2C2�ĵ���ʽ__________��
(3)�ں����£����Ϊ2 L�ĺ��������м���һ������B���ʺ�1 mol A2C������������B(s)��A2C(g) BC(g)��A2(g)��2 min��������ѹǿ������20%����2 min��A2C�ķ�Ӧ����Ϊ________��һ��ʱ���ﵽƽ�⣬����˵����ȷ����__________��
A.����B���ʵ�������Ӧ���ʼӿ�
B.���º���ʱ�ڸ�������ͨ��Ar����Ӧ���ʼӿ�
C.������ܶȲ��ٱ仯�����жϸ÷�Ӧ�ﵽ��ƽ��
D.2 minʱ��A2C��ת����Ϊ80%
E.�����ƽ��Ħ����������ʱ���÷�Ӧ�ﵽƽ��
(4)BC��C2��DCA��Һ�п��γ�һ��ȼ�ϵ�ء��õ�صĸ�����ӦʽΪ��___________��
(5)��0.2 mol D2C2Ͷ�뵽����0.1 mol FeCl2��ˮ��Һ��ǡ�ó�ַ�Ӧ����Ӧ���ܻ�ѧ����ʽΪ��______________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������������ж��ַ�����
��1���û���̿��ԭ���� ij�о�С����ij�ܱ������м��������Ļ���̿�� NO��������Ӧ��C(s)��2NO(g) ![]() N2(g)��CO2(g) H��Q kJ��mol��1 �� T1���£���Ӧ���е���ͬʱ���ø����ʵ�Ũ�Ȳ����������£�
N2(g)��CO2(g) H��Q kJ��mol��1 �� T1���£���Ӧ���е���ͬʱ���ø����ʵ�Ũ�Ȳ����������£�

��0��10 min �ڣ� N2 ��ƽ����Ӧ���� ��(N2)=________ �� T1��ʱ���÷�Ӧ��ƽ�ⳣ�� K=_____��
��30 min ����ֻ�ı�һ����������Ӧ���´ﵽƽ��ʱ�����ʵ�Ũ�����ϱ���ʾ����ı������������____________ (����ĸ)
a. ����һ�����Ļ���̿ b. �ı䷴Ӧ��ϵ���¶�
c. ��С��������� d. ͨ��һ������ NO
���� 30 min �������¶��� T2�������´ﵽƽ��ʱ�������� NO�� N2�� CO2 ��Ũ��֮��Ϊ 7��3��3����÷�Ӧ��H______0���������� �� �� ���� ���������� ��
��2��NH3 ����ԭ���� ԭ����ͼ��ʾ
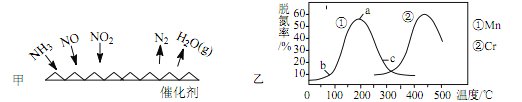
���������� c(NO2)�� c(NO)=1��1��������ͼ����ʾ���ѵ���Ӧʱ����Ӧ������ת�� 1.5mol ����ʱ�ų�������Ϊ 113.8 kJ���������ѵ���Ӧ���Ȼ�ѧ����ʽΪ_____ ��
��ͼ������һ��ʱ���ڣ�ʹ�ò�ͬ���� Mn �� Cr �ڲ�ͬ�¶��¶�Ӧ���ѵ��ʣ���ͼ��֪��ҵʹ�õ���Ѵ�������Ӧ�¶ȷֱ�Ϊ_____ ��ʹ�� Mn ������ʱ���ѵ��� b~a �γ�����ͼ�仯�Ŀ���ԭ����_____��
��3����֪������ Ka1(H2SO3)=1.810��2�� Ka2(H2SO3)=6.010��9�� ����β���е� SO2 ��ʯ��ˮ�����գ����ɵ� CaSO3 ��Һ pH��9.0������ SO32���ĵڶ���ˮ�⣬��Ksp(CaSO3)=_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Ӫ��Ԫ��֮һ������������Ȼ���й㷺���ڣ�ѭ����ϵ����ͼ��ʾ:
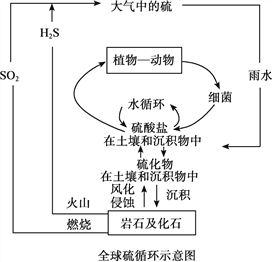
��1����ɽ�緢����H2S�ڴ������з������·�Ӧ��
��2H2S��g��+O2��g��=2S��g��+2H2O��g�� ��H=��442.38kJ/mol
��S(g)+O2(g)=SO2(g) ��H=��297.04kJ/mol��
H2S��g����O2(g)��Ӧ����SO2(g)��H2O��g�����Ȼ�ѧ����ʽ��__________��
��2����Ȼ��ر���ԭ��ͭ�����ᆳ�������������ú���CuSO4��Һ�������������������ܵ�ZnS������ת��Ϊͭ����CuS������ӳ����ܽ�ƽ��ĽǶȽ�����ZnSת��ΪCuS�Ĺ���__________��
��3����ʯȼ��ȼ��ʱ�������SO2�ķ��������������Ⱦ�������ж��ַ���������SO2���ѳ���
�ٰ������÷�����һ�ָ�Ч�ͺ��ܵ�ʪ������ʽ�����ð�ˮ���շ����е�SO2�����ڸ�������������Ϊ����泥��õ����ʲ�Ʒ����Ӧ�Ļ�ѧ����ʽ��__________��
��NaClO������Һ���շ�����ҵ�Ͽ���NaClO������Һ����SO2����Ӧ���ӷ���ʽ��__________��Ϊ���������Ч�ʣ�����Ni2O3��Ϊ�������ڷ�Ӧ�����в������ļ�����ԭ�������м�ǿ����������,�ɼӿ��SO2�����ա��ô����̵�ʾ��ͼ����ͼ��ʾ��
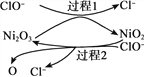
����1��Ni2O3 +ClO- = 2NiO2 +Cl-������2�����ӷ���ʽ��__________��
Ca(ClO)2Ҳ����������������Ч����NaClO���ã�ԭ����__________��
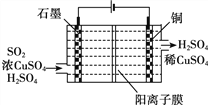
�۵绯ѧ����ij�ֵ绯ѧ����װ������ͼ��ʾ���������ѳ�SO2���ɵõ�Cu���������з����ܷ�Ӧ�����ӷ���ʽ��__________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com