
分析 (1)根据方程式①②可计算出氯乙烯的理论产量,再根据两步反应的产率进行计算氯乙烯的产量,根据反应②可计算出氯化氢的产量;
(2)根据新工艺既不需要购进氯化氢为原料,又没有副产物氯化氢剩余即反应②中产生的氯化氢等于反应③中消耗的氯化氢,结合三个反应的产率进行列等式计算.
解答 解:(1)根据CH2=CH2~CH2Cl-CH2C1~CH2=CHCl~HCl的关系可知,氯乙烯的理论产量为2.8t×$\frac{62.5}{28}$t=6.25t,所以实际产量为6.25t×98%×95%=5.8t,同时得到副产物HCl的实际产量为2.8t××98%×95%×$\frac{36.5}{28}$t=3.4t,
故答案为:5.8;3.4;
(2)设投入反应①、③的乙烯物质的量分别为x、y,则:由反应①生成的二氯乙烷为x•a%,由反应③生成的二氯乙烷为y•c%,
所以由反应①、③共制得二氯乙烷的物质的量为(x•a%+y•c%),通过反应②可获得HCl的物质的量为(x•a%+y•c%)•b%,据题意,反应③消耗的HCl为2•y•c%,
则有2•y•c%=(x•a%+y•c%)•b%,解得:$\frac{x}{y}$=$\frac{200c-bc}{ab}$,所以反应①、③中乙烯的投料比应为$\frac{200c-bc}{ab}$,
答:反应①、③中乙烯的投料比应为$\frac{200c-bc}{ab}$.
点评 本题主要考查根据有机反应的计算,难度中等,根据化学方程式计算是化学学科中最为常见的题型之一,解题时最主要的是根据题意找出等量关系.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 转移溶液时使用的烧杯未洗涤 | B. | 定容时俯视读取刻度线 | ||
| C. | 原容量瓶洗净后未干燥 | D. | 转移时有少量溶液流出瓶外 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | I | II | III |
| 实验 |  |  |  |
| 现象 | 有白色沉淀生成,滤液为蓝色 | 有白色沉淀生成,滴加稀硝酸,沉淀不溶解 | |
| 化学方程式 | 2AgNO3+CuCl2═2AgCl↓+Cu(NO3)2 | ||
| 离子方程式 | Ba2++SO42-═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题




 +2Cu(OH)2+NaOH$\stackrel{△}{→}$
+2Cu(OH)2+NaOH$\stackrel{△}{→}$ +Cu2O↓+3H2O.
+Cu2O↓+3H2O. .
.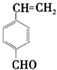 和
和 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溶液一定显碱性 | B. | 溶液不可能显碱性 | ||
| C. | 溶液可能显碱性 | D. | 溶液不可能显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NaHCO3和Na2O2 | B. | 铝粉和NaOH | C. | Na2SO3和SO3 | D. | Na2CO3和P2O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com