
| A、M>N>P>Q |
| B、P>M>N>Q |
| C、N>Q>P>M |
| D、M>P>Q>N |


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
A、用石墨电极电解MgCl2饱和溶液的总反应为:Mg2++2Cl-
| ||||
| B、精炼铜过程中阴极增重6.4g时,电路中转移电子数大于0.2NA | ||||
| C、氢氧酸性燃料电池放电时,正极反应为:O2+4e-+4H+=2H2O | ||||
| D、铅蓄电池在放电过程中,负极质量增加,正极质量增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该碳氮化合物呈片层状结构 |
| B、该碳氮化合物呈立体网状结构 |
| C、该碳氮化合物中C-N键键长大于金刚石中C-C键键长 |
| D、相邻主族非金属元素形成的化合物的硬度比单质小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 配料 | 氯化钠(NaCl)、碘酸钾(KlO3) |
| 含碘量 | 20-40mg.kg-1 |
| 保质期 | 18个月 |
| 使用方法 | 勿长时间炖炒 |
| 贮藏指南 | 避热、避光、密封、防潮 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
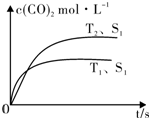
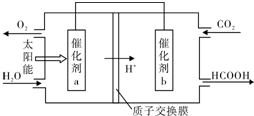
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
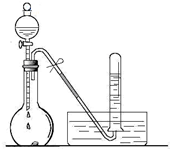 某校化学实验小组同学进行有关NO2气体的系列实验.
某校化学实验小组同学进行有关NO2气体的系列实验.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com