
 磷单质及其化合物有广泛应用.
磷单质及其化合物有广泛应用.分析 (1)三聚磷酸可视为三个磷酸分子之间脱去两个水分子的产物,即磷酸分子间两个羟基脱去应该水分子;三聚磷酸钠可以看作三聚磷酸中五个羟基的氢原子换成钠离子;
(2)①根据化合物中总化合价为0计算出P元素的化合价;
②残缺离子方程式的配平,注意得失电子守恒,配平后一定要检查电荷是否守恒.
解答 解:(1)磷酸分子间通过羟基脱水形成三聚磷酸,所以三聚磷酸的结构式为: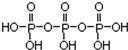 ;三聚磷酸中羟基的氢原子被钠离子取代生成三聚磷酸钠(俗称“五钠”),所以三聚磷酸钠的化学式为:Na5P3O10,
;三聚磷酸中羟基的氢原子被钠离子取代生成三聚磷酸钠(俗称“五钠”),所以三聚磷酸钠的化学式为:Na5P3O10,
故答案为:Na5P3O10;
(2)①NaH2PO2中,总化合价为0,其中钠元素为+1价,氧元素为-2价,则P元素的化合价为:+1价,
故答案为:+1;
②根据得失电子守恒:镍元素的化合价降低了2价,磷元素的化合价升高的2价,所以根据原子守恒结合电荷守恒可得配平的方程式为:H2O+Ni2++H2PO2-+═Ni+H2PO3-+2H+,
故答案为:2;1;H2O;2;1;2H+.
点评 本题考查了物质化学式的书写,氧化还原反应方程式的配平,明确三聚磷酸分子结构及性质,熟悉氧化还原反应得失电子、原子个数守恒是解题关键,题目难度不大.


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{53}^{131}$I的化学性质与${\;}_{53}^{127}$I相同 | |
| B. | ${\;}_{53}^{131}$I的原子序数为53 | |
| C. | ${\;}_{53}^{131}$I的原子核外电子数为78 | |
| D. | ${\;}_{53}^{131}$I的原子核内中子数多于质子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用醋酸溶解大理石:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| B. | 向氯化铝溶液中滴加过量氨水:Al3++4NH3•H2O=AlO2-+4NH4++2H2O | |
| C. | 向碳酸氢钙溶液中加入少量烧碱溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+H2O | |
| D. | 亚硫酸钠溶液中滴加酸性高锰酸钾溶液:5SO32-+6H++2MnO4-=5SO42-+2Mn2++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
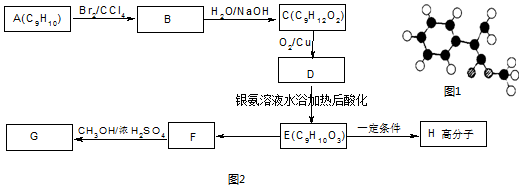
 ,G的一种同分异构体的结构简式为
,G的一种同分异构体的结构简式为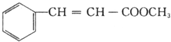 .
.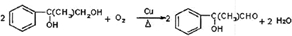
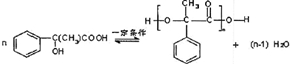 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

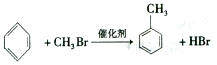 ;②C物质苯环上一卤代物只有两种.
;②C物质苯环上一卤代物只有两种. .
. $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$
 +
+ $→_{△}^{浓硫酸}$H2O+
$→_{△}^{浓硫酸}$H2O+
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚乙烯是无毒高分子化合物,可用作食品包装 | |
| B. | 人体内的蛋白质不断分解,最终生成水和二氧化碳排出体外 | |
| C. | “地沟油”经过加工处理后,可以用来制肥皂和生物柴油 | |
| D. | 电子垃圾的回收利用,可减少对土壤和水源的污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | X | Y | Z |
| A | SO2 | NaClO溶液 | CO2 |
| B | 盐酸 | 浓硫酸 | Cu |
| C | NH3 | O2 | Mg |
| D | Na2O2 | H2O | SiO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
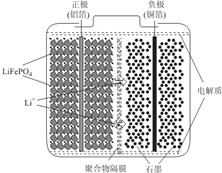 锂离子电池广泛应用于日常电子产品中,也是电动汽车动力电池的首选.正极材料的选择决定了锂离子电池的性能.磷酸铁钾(LiFePO4)以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”.
锂离子电池广泛应用于日常电子产品中,也是电动汽车动力电池的首选.正极材料的选择决定了锂离子电池的性能.磷酸铁钾(LiFePO4)以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com