
| A£® | ŗīŹĻÖĘ¼ī”¢·ŹŌķµÄÖĘČ”¹¤ŅÕ¹ż³ĢÖŠ¾łÓ¦ÓĆĮĖĪļÖŹČܽā¶ČµÄ²īŅģ | |
| B£® | Ź¹ÓĆæÉŌŁÉś×ŹŌ“”¢ÓĆ³¬ĮŁ½ē¶žŃõ»ÆĢ¼Ģę“śÓŠ»śČܼĮ”¢×¢ÖŲŌ×ӵľ¼ĆŠŌ”¢²ÉÓƵĶÄÜŗÄÉś²ś¹¤ŅÕµČ¶¼ŹĒĀĢÉ«»ÆѧµÄÄŚČŻ | |
| C£® | ŹÆÓĶ·ÖĮó”¢ĆŗµÄĘų»Æ”¢ŗ£Ė®É¹ŃĪ”¢¼īČ„ÓĶĪŪ”¢»ØÉśÖŠĢįČ”»ØÉśÓĶµČ¹ż³Ģ¶¼ŹĒĪļĄķ±ä»Æ | |
| D£® | ŗĻ½š³¬µ¼²ÄĮĻŹĒÖøČŪŗĻĮ½ÖÖ»ņĮ½ÖÖŅŌÉĻµÄ½šŹōŌŖĖŲ²¢ŠĪ³É¾ßÓŠ³¬µ¼µēŠŌµÄ³¬µ¼²ÄĮĻ£¬ČēīźŅ»īŃ£ØNb-Ti£©ŗĻ½š£¬Ķس£ĖüµÄČŪµćŅ»°ć±Č“æīŃŅŖøߣ® |
·ÖĪö A£®ŗīŹĻÖĘ¼īĄūÓƱ„ŗĶČÜŅŗÖŠĢ¼ĖįĒāÄĘČܽā¶ČŠ”Īö³ö£¬·ŹŌķµÄÖĘČ”¹¤ŅÕ¹ż³ĢÖŠ¼ÓNaCl½µµĶøß¼¶Ö¬·¾ĖįŃĪµÄČܽā¶Č£»
B£®ÓĆ³¬ĮŁ½ē¶žŃõ»ÆĢ¼Ģę“śÓŠ»śČܼĮ£¬¼õÉŁĪŪČ¾£»
C£®ĆŗµÄĘų»ÆÉś³ÉCOŗĶĒāĘų£¬¼īČ„ÓĶĪŪ·¢ÉśĖ®½ā·“Ó¦£»
D£®ŗĻ½šµÄČŪµć±ČĘäø÷×é·ÖµÄµĶ£¬Ó²¶Č±ČĘäø÷³É·Ö“ó£®
½ā“š ½ā£ŗA£®ŗīŹĻÖĘ¼īĄūÓƱ„ŗĶČÜŅŗÖŠĢ¼ĖįĒāÄĘČܽā¶ČŠ”Īö³ö£¬·ŹŌķµÄÖĘČ”¹¤ŅÕ¹ż³ĢÖŠ¼ÓNaCl½µµĶøß¼¶Ö¬·¾ĖįŃĪµÄČܽā¶Č£¬Ōņ¾łÓ¦ÓĆĮĖĪļÖŹČܽā¶ČµÄ²īŅģ£¬¹ŹAÕżČ·£»
B£®ÓĆ³¬ĮŁ½ē¶žŃõ»ÆĢ¼Ģę“śÓŠ»śČܼĮ£¬¼õÉŁĪŪČ¾£¬Ōņ×¢ÖŲŌ×ӵľ¼ĆŠŌ”¢²ÉÓƵĶÄÜŗÄÉś²ś¹¤ŅÕµČ¶¼ŹĒĀĢÉ«»ÆѧµÄÄŚČŻ£¬¹ŹBÕżČ·£»
C£®ĆŗµÄĘų»ÆÉś³ÉCOŗĶĒāĘų£¬¼īČ„ÓĶĪŪ·¢ÉśĖ®½ā·“Ó¦£¬¾łĪŖ»Æѧ±ä»Æ£¬¶ųŹÆÓĶ·ÖĮó”¢ŗ£Ė®É¹ŃĪ”¢»ØÉśÖŠĢįČ”»ØÉśÓĶµČ¹ż³Ģ¶¼ŹĒĪļĄķ±ä»Æ£¬¹ŹC“ķĪó£»
D£®ŗĻ½š³¬µ¼²ÄĮĻŹĒÖøČŪŗĻĮ½ÖÖ»ņĮ½ÖÖŅŌÉĻµÄ½šŹōŌŖĖŲ²¢ŠĪ³É¾ßÓŠ³¬µ¼µēŠŌµÄ³¬µ¼²ÄĮĻ£¬µ«ŗĻ½šµÄČŪµć±ČĘäø÷×é·ÖµÄµĶ£¬Ó²¶Č±ČĘäø÷³É·Ö“󣬹ŹD“ķĪó£®
¹ŹŃ”CD£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄŠŌÖŹ”¢Ó¦ÓĆ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕĪļÖŹµÄ×é³É”¢ŠŌÖŹ”¢Ó¦ÓĆĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬עŅā»ÆѧÓėÉś»īµÄĮŖĻµ£¬ĢāÄæÄŃ¶Č²»“ó£®


 ĆūŠ£ĮŖĆĖæģĄÖæĪĢĆĻµĮŠ“š°ø
ĆūŠ£ĮŖĆĖæģĄÖæĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | M1²”¶¾ÖŠµÄC”¢H”¢O”¢N”¢SŌŖĖŲ×īÓŠæÉÄÜŅŌ¹²¼Ū¼ü½įŗĻ | |
| B£® | M1²”¶¾ŌŚøßĪĀĻĀŅ²¾ßÓŠÉśĪļ»īŠŌ | |
| C£® | M1²”¶¾ČÜŅŗÄܲśÉś¶”“ļ¶ūŠ§Ó¦ | |
| D£® | M1²”¶¾ŌŚÉśĪļĢåÄŚĖ®½āµÄÖÕ²śĪļÖŠŗ¬ÓŠ°±»łĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
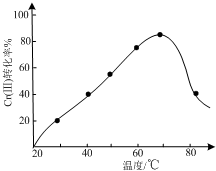 ¹¤Ņµŗ¬øõ·ĻĖ®µÄ“¦ĄķŌĄķŹĒ½«Cr2O72-×Ŗ»ÆĪŖCr3+£¬ŌŁ½«Cr3+×Ŗ»ÆĪŖCr£ØOH£©3³Įµķ£®ĄūÓĆĮņĖį¹¤Ņµ·ĻĘųÖŠµÄSO2“¦Ąķŗ¬øõ·ĻĖ®£¬¼Č³ä·ÖĄūÓĆ׏Ō“”¢ŅŌ·ĻÖĪ·Ļ£¬»¹ÄܽŚŌ¼Éś²ś³É±¾£®
¹¤Ņµŗ¬øõ·ĻĖ®µÄ“¦ĄķŌĄķŹĒ½«Cr2O72-×Ŗ»ÆĪŖCr3+£¬ŌŁ½«Cr3+×Ŗ»ÆĪŖCr£ØOH£©3³Įµķ£®ĄūÓĆĮņĖį¹¤Ņµ·ĻĘųÖŠµÄSO2“¦Ąķŗ¬øõ·ĻĖ®£¬¼Č³ä·ÖĄūÓĆ׏Ō“”¢ŅŌ·ĻÖĪ·Ļ£¬»¹ÄܽŚŌ¼Éś²ś³É±¾£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 920 kJ | B£® | 557 kJ | C£® | 436 kJ | D£® | 188 kJ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ·“Ó¦¢ŪµÄĄė×Ó·½³ĢŹ½ĪŖ5Br-+BrO3-+6H+ØT3Br2+3H2O | |
| B£® | ¢Ś¢ŪµÄÄæµÄŹĒø»¼Æä壬ĢįøßBr2µÄÅØ¶Č | |
| C£® | ÕōĮóĖžĪĀ¶ČæŲÖĘŌŚ90”ę×óÓŅµÄŌŅņŹĒ·ĄÖ¹ĪĀ¶Č¹żøß½«Ė®ÕōĮó³öĄ“ | |
| D£® | “Óŗ£Ė®ÖŠĢįČ”ČĪŗĪ»ÆѧĪļÖŹ¶¼ŠčŅŖ¾¹ż»Æѧ±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2SO2£Øg£©+02£Øg£© $?_{500”ę}^{V_{2}O_{5}}$2SO3£Øg£©”÷H=-196.6 kJ/mol£¬Ōņ2molSO2ĶźČ«·“Ó¦·Å³öČČĮæµČÓŚ196.6kJ | |
| B£® | ”°±ł£¬Ė®ĪŖÖ®£¬¶ųŗ®ÓŚĖ®”±ĖµĆ÷ĻąĶ¬ÖŹĮæµÄĖ®ŗĶ±łĻą±Č½Ļ£¬±łµÄÄÜĮæøß | |
| C£® | ŅŃÖŖC£Øs£¬ŹÆÄ«£©=C£Øs£¬½šøÕŹÆ£©”÷H=+1.9 kJ/mol£¬Ōņ½šøÕŹÆ±ČŹÆÄ«ĪČ¶Ø | |
| D£® | ĒāĘųµÄČ¼ÉÕČČĪŖ285.8 kJ/mol£¬ŌņĒāĘųČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗ2H2£Øg£©+O2£Øg£©ØT2H2O£Øl£©”÷H=-285.8 kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
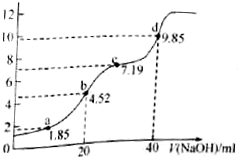 ŅŃÖŖ£ŗpKa=-LgKa£¬25”ꏱ£¬H2SO3µÄpKa1=1.85£¬pKa2=7.19£®ÓĆ0.1mol/L NaOHČÜŅŗµĪ¶Ø20mL0.1mol/L H2SO3ČÜŅŗµÄµĪ¶ØĒśĻßČēĶ¼ĖłŹ¾£ØĒśĻßÉĻµÄŹż×ÖĪŖpH£©£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
ŅŃÖŖ£ŗpKa=-LgKa£¬25”ꏱ£¬H2SO3µÄpKa1=1.85£¬pKa2=7.19£®ÓĆ0.1mol/L NaOHČÜŅŗµĪ¶Ø20mL0.1mol/L H2SO3ČÜŅŗµÄµĪ¶ØĒśĻßČēĶ¼ĖłŹ¾£ØĒśĻßÉĻµÄŹż×ÖĪŖpH£©£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | aµćĖłµĆČÜŅŗÖŠ£ŗ2c£ØH2SO3£©+c£ØSO32-£©£¼0.1 mol/L | |
| B£® | bµćĖłµĆČÜŅŗÖŠ£ŗc£ØH2SO3£©+c£ØH+£©=c£ØSO32-£©+c£ØOH-£© | |
| C£® | CµćĖłµĆČÜŅŗÖŠ£ŗ2c£ØNa+£©=3c£ØHSO3-£© | |
| D£® | dµćĖłµĆČÜŅŗÖŠ£ŗc£ØNa+£©£¾c£ØSO32-£©£¾c£ØHSO3-£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚ101 k PaŹ±£¬1 mol CÓėŹŹĮæO2·“Ӧɜ³É1mol COŹ±£¬·Å³ö110.5 kJČČ Į棬ŌņCµÄČ¼ÉÕČČĪŖ110.5 kJ/mol | |
| B£® | ŌŚ10l k PaŹ±l mol H2ĶźČ«Č¼ÉÕÉś³ÉŅŗĢ¬Ė®·Å³ö285.8 kJČČĮ棬H2Č¼ÉÕČČĪŖ-285.8KJ/mol | |
| C£® | ¼ų¶ØHClŗĶNaOH·“Ó¦µÄÖŠŗĶČČŹ±£¬Ćæ“ĪŹµŃé¾łÓ¦²āĮæ3øöĪĀ¶Č¼“ŃĪĖįĘšŹ¼ĪĀ¶Č”¢NaOHĘšŹ¼ĪĀ¶ČŗĶ·“Ó¦ŗóÖÕÖ¹ĪĀ¶Č | |
| D£® | ŌŚĻ”ČÜŅŗÖŠ£ŗH+£Øaq£©+OH-£Øaq£©=H2O£Øl£©”÷H=-57.3KJ/mol£¬Čō½«ŗ¬0.5molH2SO4µÄÅØĮņĖįÓėŗ¬1mol NaOHµÄČÜŅŗ»ģŗĻ£¬·Å³öµÄČČĮæµČÓŚ57.3KJ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com