
| X | Y | Z | |
| I1 | 496 | 738 | 577 |
| I2 | 4562 | 1451 | 1817 |
| I3 | 6912 | 7733 | 2754 |
| I4 | 9540 | 10540 | 11578 |
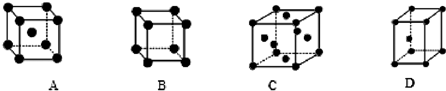
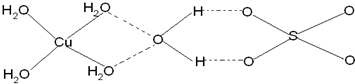
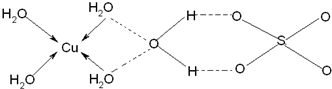 ,
, .
.

科目:高中化学 来源: 题型:
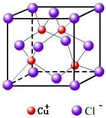 下列是部分金属元素的电离能
下列是部分金属元素的电离能| X | Y | Z | |
| 第一电离能(kJ/mol) | 520.2 | 495.8 | 418.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| X | 578 | 1817 | 2754 | 11578 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 496 | 4562 | 6912 | 9543 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(15分)1、已知X、Y、Z、W为四种短周期主族元素,它们的原子序数依次增大,其中X、Y、W位于不同周期,Y是形成化合物种类最多的元素,Z可形成![]() 型化合物,常温下W的单质为气态。
型化合物,常温下W的单质为气态。
(1)由X、Y组成的最简单化合物可作为某燃料电池的 极反应物。
(2)化合物![]() 所含化学键种类为 ,属于 化合物(填“离子”或“共价”)。
所含化学键种类为 ,属于 化合物(填“离子”或“共价”)。
(3)写出实验室制备W单质的化学方程式为 。
Ⅱ、铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1) 黄铁矿(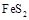 )是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
![]() ,有3mol
,有3mol![]() 参加反应,转移 mol电子。
参加反应,转移 mol电子。
(2) 氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为
;从腐蚀废液回收得到金属铜,还需要的试剂是 。
(3) 与明矾相似,硫酸铁也可用作净水剂,其原理是
(4)钢铁的电化腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山东省高三第二次质量检测化学试卷 题型:填空题
(15分)1、已知X、Y、Z、W为四种短周期主族元素,它们的原子序数依次增大,其中X、Y、W位于不同周期,Y是形成化合物种类最多的元素,Z可形成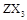 型化合物,常温下W的单质为气态。
型化合物,常温下W的单质为气态。
(1)由X、Y组成的最简单化合物可作为某燃料电池的 极反应物。
(2)化合物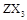 所含化学键种类为 ,属于 化合物(填“离子”或“共价”)。
所含化学键种类为 ,属于 化合物(填“离子”或“共价”)。
(3)写出实验室制备W单质的化学方程式为 。
Ⅱ、铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)
黄铁矿(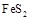 )是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
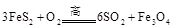 ,有3mol
,有3mol 参加反应,转移
mol电子。
参加反应,转移
mol电子。
氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为 ;从腐蚀废液回收得到金属铜,还需要的试剂是 。
(2) 与明矾相似,硫酸铁也可用作净水剂,其原理是 。
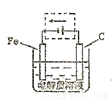
(4)钢铁的电化腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com