
【题目】已知:X(g)+2Y(g)![]() 3Z(g) H=﹣a kJ·molˉ1(a>0)。下列说法不正确的是( )
3Z(g) H=﹣a kJ·molˉ1(a>0)。下列说法不正确的是( )
A. 0.1 mol X和0.2 mol Y充分反应生成Z,放出能量一定小于0.1 a kJ
B. Y的起始浓度不能为零,平衡浓度也不能为零
C. 在其他条件不变的情况下,降低反应温度,正、逆反应速率均减小,平衡会发生移动
D. 当反应达到平衡状态时,一定存在3v(Y)正=2v(Z)逆
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源: 题型:
【题目】假设氨基酸的平均相对分子质量为128,现有一蛋白质分子由两条多肽链组成,具有肽键98个,此蛋白质的相对分子质量是( )
A. 12800 B. 12544 C. 11036 D. 12288
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【江西省师范大学附属中学2017届第三次模拟考试】CO2经催化加氢可合成乙烯:2CO2 (g) +6H2 (g) ![]() C2H4(g)+4H2O(g)。0.1 MPa时,按n(CO2):n(H2)=l:3投料,测得不同温度下平衡时体系中各物质浓度的关系如图。下列叙述不正确的是
C2H4(g)+4H2O(g)。0.1 MPa时,按n(CO2):n(H2)=l:3投料,测得不同温度下平衡时体系中各物质浓度的关系如图。下列叙述不正确的是
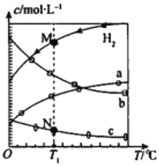
A.该反应的△H<0
B.曲线b代表H2O
C.N点和M点所处状态的c(H2)不一样
D.其它条件不变,T1℃、0.2 MPa下反应达平衡时c(H2)比M点大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质的性质判断不正确的是
A.12g金刚石中含有C一C键的个数为2NAB.键的极性:HF>H2O
C.水中的溶解性:CH3COOH>HCOOCH3D.键角:CO2>SO2>H2O>NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【葫芦岛协作体2017届下学期模拟考试(6月)】金属(M)-空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH)n。己知:电池的 “理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法不正确的是( )
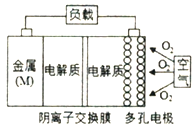
A.采用多孔电极的目的是提髙电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
B.比较Mg、Al、Zn三种金属一空气电池,Al -空气电池的理论比能量最高
C.M-空气电池放电过程的正极反应式:4Mn++nO2+2nH2O+4ne-=4M(OH)n
D.在M-空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课题组设计实验探究SO2的性质。

实验现象:B中无沉淀生成,C中有白色沉淀;D中溶液颜色变浅,E中产生白色沉淀。
(1)仪器R的名称是______________________。
(2)实验室在常温下用80%的硫酸与亚硫酸钠粉末反应制备SO2,写出A中反应的化学方程式:______________________________________。
(3)部分实验步骤如下:连接装置、检查气密性、装药品,向装置中通入一段时间N2,然后启动A中反应。“通入一段时间的N2”的目的是___________________________。
(4)探究装置C中通入SO2的量与产物的关系。
①他们提出如下猜想:
猜想1:通入过量的SO2,则发生反应的离子方程式为Ba2++2NO3-+3SO2+2H2O=BaSO4↓ +2SO42-+2NO+4H+。
猜想2:通入少量的SO2,则发生反应的离子方程式为______________________。
②请你帮他们设计实验证明猜想1和猜想2哪个合理,完成下列实验:
提供试剂:溴水、铜粉、Ba(NO3)2溶液、BaCl2溶液、Na2CO3溶液
实验步骤 | 实验现象及结论 |
取少量C中反应后溶液于试管中,__________ | ________________ |
(5)下列可检验装置D反应后溶液中是否有Fe2+的最佳试剂是_____(填字母)。
a.KSCN溶液 b.NaOH溶液 c.K3[Fe(CN)6]溶液 d.KSCN溶液和双氧水
(6)常温下,实验完毕后,分离、提纯装置E中白色固体M,取适置M于试管中,滴少量盐酸(M剩余),所得溶液的pH_____7(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【徐州市2017届考前模拟冲刺打靶卷】利用合成气(主要成分为CO、CO2和H2)通过下列反应合成甲醇。下列说法正确的是
反应①:CO2(g) + H2(g)![]() CO(g) + H2O(g) △H1=41 kJ·mol–1
CO(g) + H2O(g) △H1=41 kJ·mol–1
反应②:CO(g) + 2H2(g)![]() CH3OH(g) △H2=–99 kJ·mol–1
CH3OH(g) △H2=–99 kJ·mol–1
反应③:CO2(g) + 3H2(g)![]() CH3OH(g) + H2O(g) △H3
CH3OH(g) + H2O(g) △H3
A.反应①为放热反应 B.增大反应①的压强,H2转化率提高
C.反应②使用催化剂,△H2不变 D.△H3=-58 kJ·mol–1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com