
“科学与技术”模块(10分)
电石浆是氯碱工业中的一种废弃物,其大致组成如 下表所示:
下表所示:
| 成分 | CaO | SiO2 | Al2O3 | Fe2O3 | MgO | CaS | 其它不溶于酸的物质 |
| 质量分数(%) | 65~66 | 3.5~5.0 | 1.5~3.5 | 0.2~0.8 | 0.2~1.1 | 1.0~1.8 | 23~26 |
用电石浆可生产无水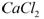 ,某化工厂设计了以下工艺流程:
,某化工厂设计了以下工艺流程:
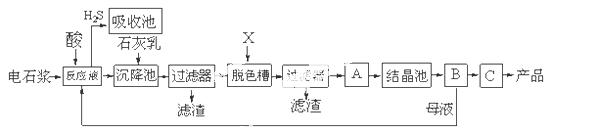
已知氯化钙晶体的化学式是:CaCl2·6H2O;H2S是一种酸性气体,且具有还原性。
(1)反应器中 加入的酸应选用 。
加入的酸应选用 。
(2)脱色槽中应加入的物质X是 ‚ ;设备A的作用是 ƒ ;设备B的名称为 ④ ;设备C的作用是 ⑤ 。
(3)为了满足环保要求,需将废气H2S通入吸收池,下列物质中最适合作为吸收剂的是 ⑥ 。
A.水 B.浓硫酸 C.石灰乳 D.硝酸
(4)将设备B中产生的母液重新引入反应器的目的是 ⑦ 。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
德国人弗里茨·哈勃由于发明了合成氨的方法而获得诺贝尔化学奖,他的发明大大提高了农作物的产量同时也提高了硝酸、炸药的产量。下列说法中正确的是( )
A.氨气遇到浓盐酸会发生反应产生白烟
B.氨水显酸性
C.N2和H2在点燃或光照条件下可合成氨
D.由氨制取硝酸过程中,氮元素被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关金属的工业制法中正确的是 ( )
A.制钛:用金属钠置换氯化钛(TiCl4)溶液中的钛
B.炼铁:用焦炭和空气反应产生的CO在高温下还原铁矿石中铁的氧化物
C.制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液
D.炼铜:用黄铜矿经电解精炼得到纯度为99.9%的铜
查看答案和解析>>
科目:高中化学 来源: 题型:
铝的活泼性较强,直到十八世纪人类才 开始将Al从它的化合物中冶炼出来。当时铝价格十分昂贵,拿
开始将Al从它的化合物中冶炼出来。当时铝价格十分昂贵,拿
破仑的头盔就是用Al 制作的,现在还保存在大英博物馆中。下列冶炼铝的方法正确的是( )
制作的,现在还保存在大英博物馆中。下列冶炼铝的方法正确的是( )
A.Al2O3(熔融) Al
Al
B.Al2O3 AlCl3(熔融)
AlCl3(熔融) Al
Al
C.Al(OH)3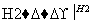 Al
Al
D.Al2O3 Al
Al
查看答案和解析>>
科目:高中化学 来源: 题型:
海水是镁的主要来源之一 。从海水中提取镁可按如下步骤进行:①把贝壳制成石灰乳;②向引入的海水
。从海水中提取镁可按如下步骤进行:①把贝壳制成石灰乳;②向引入的海水
中加入石灰乳,沉降、洗涤、过滤沉淀物;③将沉淀物与盐酸反应,结晶、过滤、干燥;④电解得到产物。
(1)以上提取镁的全过 程中,没有涉及的化学反应类型是________(填序号)。
程中,没有涉及的化学反应类型是________(填序号)。
A.分解反应 B.化合反应
C.置换反应 D.复分解反应
(2)下列关于提取镁的说法中,不正确的是______(填序号)。
A.此法的优点之一是原料来自大海
B.进行①②③步骤的目的是富集MgCl2
C.可用电解熔融氧化镁的方法制取镁
D.电解冶炼镁要消耗大量电能
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式书写正确的是( )
A.钠和冷水反应Na+2H2O===Na++2OH-+H2↑
B.金属铝溶于氢氧化钠溶液Al+2OH-===AlO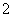 +H2↑
+H2↑
C.金属铝溶于盐酸中2Al+6H+===2Al3++3H2↑
D.铁跟稀硫酸反应Fe+2H+===Fe3++H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
某无色透明溶液与铝反应放出H2,该溶液中可能含有大量的H+、K+、Mg2+、Cl-、OH-、SO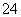 、CO
、CO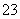 ,试推断:
,试推断:
第一种情况,无色透明溶液中一定有________,可能有__________离子。
第二种情况,无色透明溶液中一定有________,可能有__________离子。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知室温下,Al(OH)3的Ksp或溶解度远大于Fe(OH)3。向浓度均为0.1 mol·L-1的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液。下列示意图表示生成Al(OH)3的物质的量与加入NaOH溶液的体积的关系,合理的是 ( )
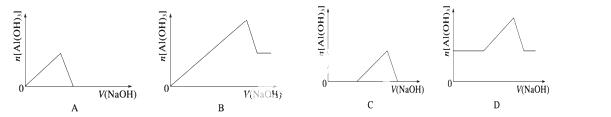
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是部分短周期元素原子(用字母表示)最外层电
子数与原子序数的关系图。下列说法正确的是 ( )
A.该图体现出原子核外电子层呈现周期性变化
B.原子半径:W>R>X
C.W的氢化物与R的氢化物水溶液的酸性比较,前者强于后者, 可证明非金属性:R>W
D.R、Z形成的化合物中可能含有共价键

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com